自閉スペクトラム症(ASD)の背景にある、遺伝子や細胞の働きについて、最新の知見にもとづいてやさしく解説します。
やさしいまとめ
自閉スペクトラム症(Autism Spectrum Disorder:ASD)は、言葉の遅れや人との関わりのむずかしさ、特定の行動や興味への強いこだわりなどがみられる発達のちがいです。このような特徴は、早い時期から見られることが多く、子ども一人ひとりで症状の出方が異なります。
近年の研究により、ASDの背景には、PTENやTSC1/TSC2といった遺伝子の変化や、mTOR経路など細胞内のシグナル伝達の異常が関わっていることが明らかになってきました。これらは、神経細胞の発達やつながり(シナプス)に影響を与えることがあり、発達の進み方に差が生まれる一因と考えられています。
この記事では、自閉スペクトラム症のしくみ、代表的な症状、関連する遺伝子や検査の情報、現在わかっている治療の選択肢、将来の見通しについて、できるだけわかりやすく丁寧にご紹介します。初めてこの診断に触れた方や、ご家族として理解を深めたい方にも、安心して読んでいただける内容を心がけています。
概要|Overview
自閉スペクトラム症(Autism Spectrum Disorder:ASD)は、遺伝的な要因、臨床的な症状、そして神経生物学的な背景が非常に多様である、複雑な神経発達障害です。ASDは、特定のひとつの原因によって起こるものではなく、複数の要因――たとえば遺伝的変異やエピジェネティックな影響(遺伝子の働き方に影響を与える仕組み)、環境的な要因――が重なり合って脳の発達、情報のやり取り、構造のまとまり方に影響を与えることで発症すると考えられています。
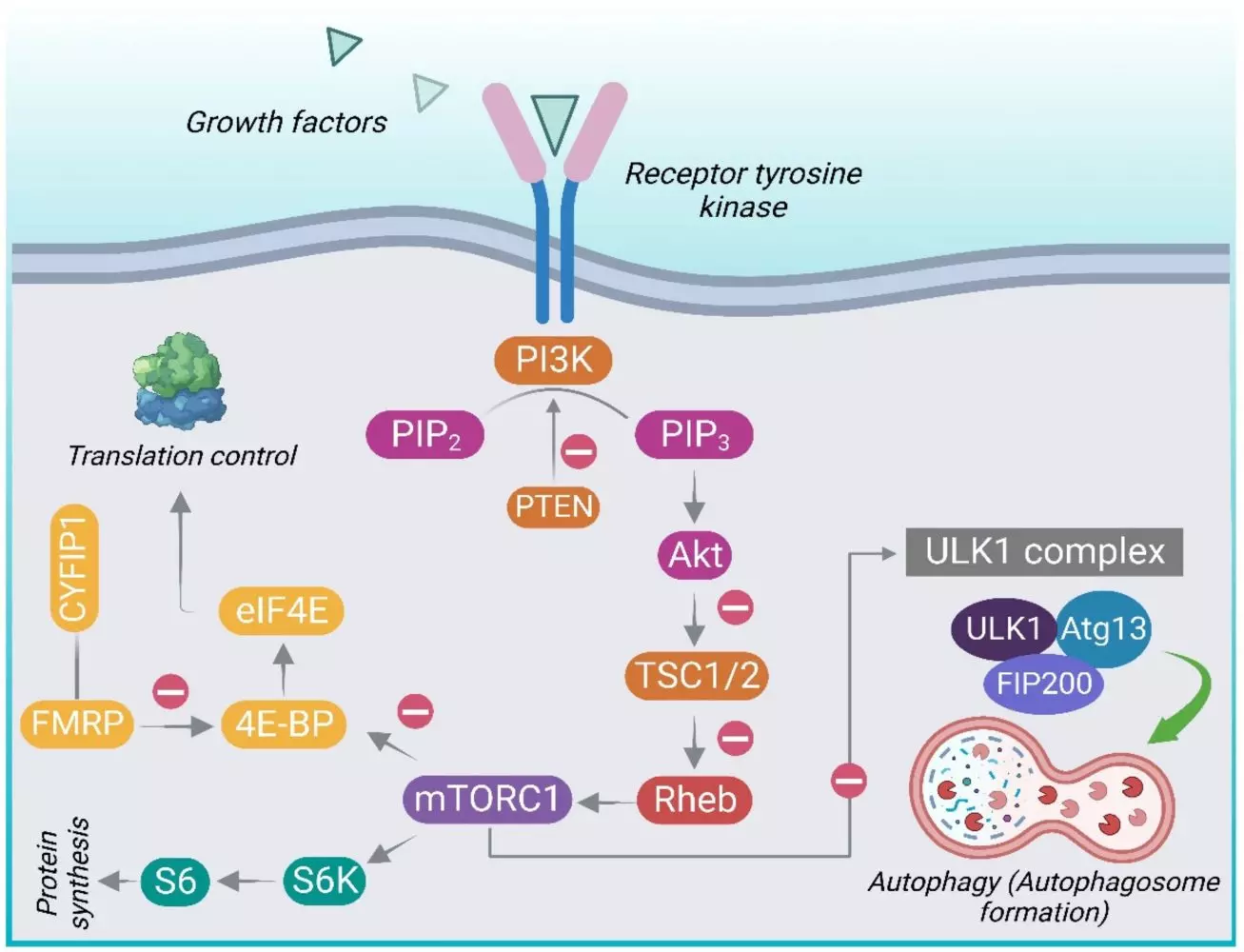
こうした複雑な要因が交わる中心的な仕組みのひとつに、「PI3K–AKT–mTOR経路(pathway)」と呼ばれる細胞内のシグナル伝達系があります。これは、脳の発達や細胞の成長を調節するうえで非常に重要な経路です。
なかでも「mTOR(mechanistic Target of Rapamycin)」というタンパク質は、セリン/スレオニンキナーゼと呼ばれる酵素で、細胞の“司令塔”のような役割を担っています。mTORは、栄養素、ホルモン、エネルギーの状態、インスリンやIGF-1(インスリン様成長因子1)などの成長因子からのシグナルを受け取り、細胞がタンパク質を作る働き(タンパク質合成)、不要物を分解する仕組み(オートファジー)、代謝、細胞の増殖などを調整します。
このmTOR経路は、主に以下の2つのタンパク質複合体を介して働きます。
- mTORC1:タンパク質合成やオートファジーの制御に関わります
- mTORC2:細胞の形を支える構造(細胞骨格)や代謝のバランスを調整します
もともとこの経路はがんや細胞増殖に関係するとして研究が進められてきましたが、近年では脳の発達過程においても極めて重要な役割を果たしていることがわかってきました。たとえば、神経細胞のサイズ、樹状突起(情報を受け取る部分)の構造、シナプス(神経同士のつながり)の働き、そして神経回路の形成などを調整していることが報告されています。
この経路が正しく働かないと、ASDの発症に関わるさまざまな問題が起こることがわかっています。たとえば、PI3K–AKT–mTOR経路の上流にあるPTEN、TSC1/TSC2、FMR1などの遺伝子や、下流のEIF4E、RHEBといった遺伝子に変異が起こると、この経路の働きが乱れやすくなります。特に、mTORC1の活動が過剰になると、不要なシナプスの剪定がうまく進まず、神経細胞の突起が過剰に伸びたり、頭囲(頭の大きさ)が大きくなる(巨頭症)などの変化が生じることがあり、これらはASDでよく見られる特徴のひとつです。
また、この経路はMAPK/ERK経路、Hedgehog経路、NF-κB経路など、他の重要なシグナル伝達経路ともつながっており、脳の発達全体にわたる“ハブ”のような働きをしていると考えられています。
一見まったく異なる病気のように思えるASDとがんですが、実は共通する分子的な仕組みを持っていることがわかってきました。たとえば、がんを引き起こす体細胞の変異(体の細胞に生じる変異)を起こすPTEN、PIK3CA、BRAFなどの遺伝子が、発生初期の胚の段階で変異すると、神経発達の異常(NDDs)を引き起こす可能性があるのです。
同じ遺伝子変異であっても、それが「いつ」「どの細胞で」「どのくらい強く」「どのような染色体の状態で」起きるかによって、がんのように細胞の増殖が過剰になる場合もあれば、ASDのように細胞の分化やシナプス形成がうまく進まない場合もあります。
脳は、非常に複雑で繊細な構造と代謝的なニーズを持っているため、シグナルの強さやタイミングにほんのわずかなズレがあるだけでも大きな影響を受けやすいと考えられています。このことが、一部のNDDのある方において、がんの発症リスクがやや高いことの一因とされており、共通の遺伝的背景が、病気の現れ方によって異なる形で表出している可能性があります。
このように、ASDは単なる行動の障害ではなく、分子レベルでの複雑な異常が重なって起きる、全身的な発達障害なのです。PI3K–AKT–mTOR経路は、細胞レベルの情報のやり取りがどのように脳の構造や機能に変換されるのかを理解するための中心的な鍵となっています。そしてこの経路を探究することで、ASDやその他の神経発達症の病態理解だけでなく、将来的な治療法の開発にもつながる可能性が期待されています。
遺伝子領域|Implicated Genomic Region
このレビューで取り上げられている神経発達障害(Neurodevelopmental Disorders:NDDs)や自閉スペクトラム症(ASD)では、遺伝的な背景として、クロマチンリモデリング因子(chromatin remodelers)や、細胞内シグナル伝達経路の関連遺伝子に変異があることが明らかになっています。特に、PI3K/AKT/mTOR経路やMAPK/ERK経路といった、細胞の成長・分化・神経発達に関与する主要な経路が注目されています。
以下のような遺伝子群が、ASDやNDDでしばしば異常を認められることが報告されています:
クロマチンリモデリング因子
クロマチンとは、DNAが巻きついている構造体のことで、遺伝子の発現(オン・オフ)に大きく関わります。これらの因子に異常があると、必要な遺伝子が適切なタイミングで働かなくなるおそれがあります。
- SMARCC2(BAF170)、ARID1A、ARID1B、SMARCC1、SMARCA4
DNAにアクセスして読み取る働きを調節する因子です - CHDファミリーのヘリカーゼ群
DNAの構造を緩めて遺伝子発現を可能にする酵素で、NDDに関連するコピー数変異との関係が指摘されています
シグナル伝達経路に関わる遺伝子:
- PI3K/AKT/mTOR経路
- PTEN、PIK3CA、EIF4E、TSC1、TSC2などの遺伝子に変異が繰り返し報告されています。
- この経路は細胞の成長・代謝・シナプス形成に深く関わっており、過剰な活性や制御不全がASDに関与していると考えられています。
- MAPK経路(Mitogen-Activated Protein Kinase)
BRAFやPAK1といった遺伝子が、下流のERKシグナルを介して神経の成長や分化に影響を与えています。 - eIF4E/4E-BP1複合体
mTORC1の主要な標的であり、タンパク質翻訳を制御する働きを持っています。これによりシナプスの可塑性(神経の柔軟な働き方)が影響を受けるとされます。
これらの遺伝子の機能は、転写の制御(遺伝子からRNAへの情報写し取り)、タンパク質の合成、シナプスの発達、神経の可塑性といった、脳の正常な発達に欠かせないプロセスと深く結びついており、これらの働きが乱れることが、NDDやASDの症状として現れてくるのです。
疾患名|Disorder
本稿で取り上げられている遺伝性神経発達障害(Neurodevelopmental Disorders:NDDs)および自閉スペクトラム症(Autism Spectrum Disorder:ASD)には、さまざまな病型が含まれます。これらは単独で現れることもありますが、しばしば重複して併存する(共存する)ことがあり、背景にある遺伝的・分子的な仕組みも共通する部分が多いことがわかってきました。主な関連疾患には以下のようなものがあります。
自閉スペクトラム症(ASD:Autism Spectrum Disorder)
社会的な相互作用やコミュニケーションの困難さ、興味や行動のかたよりといった特徴がみられる発達障害です。早期の発見と支援が重要とされています。
神経発達障害(NDDs:Neurodevelopmental Disorders)
以下のような症状や状態が含まれます。
- 知的障害(Intellectual Disability)
理解力や学習能力に影響する障害で、軽度から重度まで幅があります - 注意欠如・多動症(ADHD:Attention-Deficit/Hyperactivity Disorder)
集中力が続きにくい、落ち着きがないといった特性がみられます - 学習障害(Learning Disabilities)
読み書き、計算など、特定の学習分野に困難を伴います - 言語、運動、認知の発達遅滞
話し始めるのが遅い、運動がぎこちない、思考や判断がゆっくり進むなど - てんかん(Epilepsy)
繰り返すけいれん発作が特徴です - 脳性麻痺(Cerebral Palsy)
脳の発達に関連する運動障害で、生まれつきまたは早期に発症することがあります
症候性自閉スペクトラム症(Syndromic ASD forms)
遺伝子異常を背景とする特定の症候群の一部としてASDの症状がみられるケースです。以下のような疾患が知られています。
- 脆弱X症候群(Fragile X Syndrome:FMR1遺伝子の異常)
- 結節性硬化症(Tuberous Sclerosis Complex:TSC1またはTSC2の異常)
- レット症候群(Rett Syndrome:MECP2遺伝子の異常)
- アンジェルマン症候群(Angelman Syndrome:UBE3A遺伝子の異常)
- PTENハマルトーマ腫瘍症候群(PTEN Hamartoma Tumor Syndrome)
これらの疾患では、PI3K/AKT/mTOR経路の異常活性化や制御不全が、共通の分子レベルでの特徴として認められており、症状や合併症に深く関係しています。
疫学|Epidemiology
神経発達障害(Neurodevelopmental Disorders:NDDs)および自閉スペクトラム症(Autism Spectrum Disorder:ASD)の診断件数は、ここ数十年で着実に増加しています。この増加にはさまざまな要因が影響しており、診断基準の見直しや検査法の進歩、医療や教育現場での認識の高まりが大きく関わっていると考えられています。一方で、環境的あるいは遺伝的な要因がこの傾向の背景にある可能性も、完全には否定されていません。
アメリカ合衆国における全国調査(2014年〜2019年)から得られたデータによると、ASDの診断率は5歳から17歳の小児の間で2.3%から2.9%の範囲で推移していました。すべての年齢群において、男児は女児よりも高い頻度でASDと診断される傾向が一貫して確認されています。
また、ADHD(注意欠如・多動症)の診断率も長期的に上昇しています。1997年時点では6.3%でしたが、2019年には9.9%に達しており、診断率の上昇が明確に示されています。学習障害についても、同じ年齢層の子どものうち約7.1%が該当するとの報告があり、これらの神経発達関連の診断が小児集団において一定の頻度で認められることがわかります。
特定の遺伝子変異に基づく症候群においては、さらに特徴的な表現型が観察されています。たとえばPAK1遺伝子に変異があるケースでは、中等度から重度の知的障害、巨頭症(頭囲が大きい状態)、脳室拡大、てんかん、およびASD様の行動特性が報告されています。こうした症状の組み合わせは、分子レベルでの異常がどのように神経発達に影響を及ぼすかを示すひとつの例となっています。
さらにあまり知られていない事実として、NDDのある方では、生涯を通じてがん(悪性腫瘍)を発症するリスクがわずかに高いことが、統計的に示されています。この関連には、NDDとがんの双方に共通する遺伝子レベルの変異が関与している可能性があり、同じ分子メカニズムが、発達と腫瘍形成という異なる経過に分岐する一因になっていると考えられています。
病因|Etiology
自閉スペクトラム症(ASD)や神経発達障害(NDDs)の原因(病因)はひとつに限られるものではなく、複数の要素が重なり合って発症に至ることがわかってきました。これを「多因子的(multifactorial)」といいます。具体的には、以下の4つの側面が病因として重要と考えられています。
1 遺伝的変異(Genetic Mutations)
神経発達障害の背景にある要因として、まず注目されているのは、遺伝子の働きを制御する仕組みに関わる変異です。とくに、DNAの読み取りやすさ(アクセシビリティ)を調節する「クロマチンリモデリング因子(chromatin remodeling factors)」と呼ばれるタンパク質群は、神経系の正常な発達に不可欠な役割を果たしています。
たとえば、SMARCC2、ARID1A、そしてCHDファミリーのヘリカーゼといった遺伝子群は、細胞がどの遺伝子をいつ、どの程度活性化するかを制御しており、これらの異常は神経細胞としての分化(neural lineage specification)に支障をきたす可能性があります。このような初期段階での遺伝子発現の乱れは、その後の脳の構造や機能の形成にも長期的な影響を与えると考えられています。
一方で、PTEN、TSC1、TSC2、FMR1といった遺伝子は、細胞内の情報伝達や制御の中枢に位置し、細胞の増殖速度、タンパク質合成(翻訳)、さらにはシナプスの形成(synaptogenesis)など、多くの基本的な生物学的プロセスを調整しています。これらに変異が生じた場合、シグナル伝達が過剰に活性化されたり、抑制の効かない状態に陥ったりすることがあり、その結果として神経発達に有害な影響が現れることがあります。
このように、クロマチンの構造調整と細胞内シグナル制御という二つの異なる領域における遺伝的変異が、脳の発達や機能に共通して深い関わりを持つことが、近年の研究から明らかになってきています。
2 シグナル伝達経路の異常(Pathway Dysregulation)
細胞が適切に成長し、働きを果たすためには、さまざまな情報を受け取り、それに応じて反応する仕組みが必要です。このような情報のやり取りを担う「通信網」のような役割を果たしているのが、細胞内のシグナル伝達経路です。なかでもPI3K/AKT/mTOR経路およびMAPK経路は、脳の発達において非常に中心的な働きを担っており、多くの神経発達障害との関連が指摘されています。
これらの経路に異常が起こると、いくつかの重要な発達プロセスに支障が生じます。たとえば、細胞が増殖と分化のタイミングを正しく切り替えるための細胞周期の制御が乱れたり、神経細胞としての成熟が途中で止まってしまうといった、神経分化の障害が起こることがあります。さらに、神経細胞同士の接続をつくるための構造であるシナプスの形成や機能にも影響が及び、情報のやり取りが非効率になる可能性があります。
このような分子レベルの異常は、結果として神経発達障害(NDDs)に特徴的な行動や認知の問題として現れることがあり、その発症メカニズムの重要な一因と考えられています。
3 発生時期と細胞の状態(Timing and Cellular Context)
遺伝子に変異が生じた場合、その影響の大きさや現れ方は、その変異がいつ、どこで起こるかによって大きく異なります。もし変異が生殖細胞(親から子に受け継がれる細胞)や、受精後まもない胚の初期段階で生じた場合には、脳が最も繊細にかたちづくられていく時期に直接影響を及ぼすため、神経発達障害(NDD)のリスクが高くなると考えられています。
一方で、出生後あるいは発生の後半に体細胞に変異が生じた場合は、発達よりも細胞の増殖制御の異常が目立ちやすく、がんなどの疾患につながる可能性が高いとされています。つまり、同じ遺伝子の変異であっても、その発現する時期や影響を受ける細胞の種類によって、結果として現れる病気はまったく異なる可能性があるということです。
4 エピジェネティックおよび環境的要因(Epigenetic and Environmental Influences)
遺伝子そのものの配列に変化がなくても、エピジェネティック(後成的)な調節によって、遺伝子の働き方が大きく左右されることがあります。エピジェネティクスとは、DNAの並びを変えることなく、どの遺伝子が“いつ・どれだけ”発現するかを制御する仕組みを指します。そのひとつの鍵となるのが、クロマチン構造の開閉です。クロマチンが開いている状態では、遺伝子が読み取られやすくなり、反対に閉じていると遺伝子の発現は抑えられます。このような状態のことを「染色体のアクセシビリティ(chromatin accessibility)」と呼び、遺伝子の機能発現に大きな影響を与えます。
特に発達初期の脳では、メチル化や脱メチル化といった化学的修飾が、神経発達に重要な遺伝子の発現をきめ細かく調整しています。こうした調節が乱れると、必要な遺伝子が本来働くべきタイミングや強さで機能しなくなることがあり、その結果、神経細胞の分化やネットワーク形成に影響が及び、神経発達障害の一因となる可能性があります。
症状|Symptoms
自閉スペクトラム症(ASD)やその他の神経発達障害(NDDs)では、認知、行動、神経学的な側面にわたってさまざまな症状がみられます。これらは、神経細胞のつながり(シナプス)の形成や可塑性、シグナル伝達、DNA構造の調節機能に関わる異常が関係していると考えられています。
NDDに共通する主な症状
- 知的障害(軽度から重度まで)
- 言語や話し言葉の発達の遅れ
- 学習障害(読み書きや計算が困難)
- 運動協調の問題(走る、跳ぶ、手先の操作などが苦手)
- 注意欠如・多動症(ADHD)
- 脳性麻痺(Cerebral Palsy)
- 記憶力や実行機能(段取りを組んで行動する力)の障害
- 自閉スペクトラム的な行動特性(対人関係の困難、同じ行動を繰り返す、強いこだわりなど)
ASDに特有の特徴
- 社会的な関わりやコミュニケーションの難しさ
- 繰り返しの行動や興味の限定
- 幼少期から症状が始まることが多い(通常3歳未満)
また、以下のような合併症(併存することが多い症状)もよくみられます。
- てんかん(けいれん発作)
- 不安感やいら立ちやすさ
- ジスキネジア(不随意運動)や睡眠障害
- 消化器症状(便秘や腹痛など)
- 頭囲の異常(巨頭症や小頭症)
- 脳皮質の異形成(正常な大脳の形成がうまくいかない状態)やプルキンエ細胞の消失(小脳の神経細胞)
- 興奮性と抑制性のバランスの乱れ(E/Iバランス)
症候群ごとの特徴的な所見
- PAK1遺伝子の変異
てんかん、脳室拡大、巨頭症、中等度から重度の発達遅滞が報告されています - TSC1/TSC2変異による結節性硬化症
皮膚症状、てんかん、大脳皮質の結節、ASD様の行動特性 - PTEN遺伝子の変異
「巨頭症/自閉症症候群」とも呼ばれ、認知機能障害とともにがんリスクの上昇が伴います - FMR1遺伝子の変異(脆弱X症候群)
ASD、知的障害、異常な樹状突起の構造などが報告されています
これらの症状は、単に遺伝子の変異があるというだけではなく、それによって引き起こされるタンパク質合成の異常、オートファジーの障害、シナプスの剪定の乱れといった分子レベルの異常が脳の機能に影響していることを示しています。
検査・診断|Testing & Diagnosis
自閉スペクトラム症(ASD)や関連する神経発達障害(NDDs)の診断には、発達の経過や行動の観察が重要な役割を果たします。また、必要に応じて遺伝子検査を行うことで、より正確な診断や治療方針の参考にすることができます。
臨床的評価(Clinical Evaluation)
自閉スペクトラム症(ASD)や神経発達障害(NDD)の診断では、いくつかの方法が用いられます。まず、発達の既往歴(developmental history)や保護者からの聞き取りが行われます。さらに、行動観察を通じて特性を把握することも重要です。診断には、標準化された評価ツールが使用されます。ADOS-2(Autism Diagnostic Observation Schedule)は、実際の行動を観察し、自閉スペクトラム特性を評価するための検査です。ADI-R(Autism Diagnostic Interview-Revised)は、保護者への詳細なインタビューに基づいてASDの特徴を明らかにするために用いられます。これらに加えて、認知機能や心理的発達の検査も併用されます。
遺伝子検査(Genetic Testing)
ASDやNDDでは、親から受け継いだ遺伝子の変異や、新しく生じた(de novo)変異が関与していることが多く、遺伝子検査が重要な手がかりとなる場合があります。主に次のような検査が行われます。
- 染色体マイクロアレイ(CMA:Chromosomal Microarray)
微細な染色体のコピー数変化(重複や欠失)を検出します。 - 全エクソーム解析(WES:Whole-Exome Sequencing)
遺伝子の“設計図”の中でも、タンパク質を作る部分(エクソン)を網羅的に調べる方法です。 - 特定の遺伝子パネル検査(Targeted Panel Testing)
ASDやNDDに関与が知られている遺伝子(PTEN、TSC1/TSC2、FMR1、EIF4Eなど)を集中的に調べます。
ある大規模データベース(de novo-db)からの報告によると、約14,133件の点変異が7,907種類の遺伝子で確認されました。このうち、712個の転写因子(遺伝子のスイッチを入れる役割)と、50種類のクロマチンリモデリング因子が関連していました。また、PI3K/mTOR経路に関連する遺伝子では239件、MAPK経路では159件の変異が確認されています。
分子・機能的なバイオマーカー(Molecular and Functional Biomarkers)
現在のところ、血液や脳脊髄液で測定可能な標準的なバイオマーカー(生物学的指標)は確立されていません。しかし、研究段階ではいくつかの指標が検討されています。mTOR経路の活性を示すものとして、S6、4E-BP1、eIF4Eのリン酸化状態が挙げられます。また、オートファジー関連マーカーとしては、LC3-IIやp62などが対象とされています。さらに、MRIによる脳の過成長や皮質異形成の画像所見も評価項目として用いられています。現在も、非侵襲的(からだに負担の少ない)バイオマーカーを活用した診断や経過観察の方法について、世界中で研究が続けられています。
治療法と管理|Treatment & Management
神経発達障害や自閉スペクトラム症に対しては、現時点では確立された「治癒」手段は存在しません。しかし、症状を和らげ、生活の質を高めるための支援や治療法が数多く開発されており、できるだけ早い時期からの介入がより良い経過につながることが知られています。
治療は、行動療法、言語・作業療法、薬物療法、そして分子標的治療(特定の経路をねらった薬)など、多方面からのアプローチが行われます。
行動療法(Behavioral Interventions)
行動療法としては、いくつかの方法が用いられています。応用行動分析(ABA:Applied Behavior Analysis)は、行動の強化・改善を促す療育であり、科学的な根拠に基づいた支援方法です。言語療法および作業療法は、コミュニケーションや日常生活動作の発達を支援する目的で行われます。また、社会的スキル訓練や特別支援教育は、対人関係や学校生活における困難をやわらげることを目指して実施されます。
薬物療法(Pharmacologic Interventions)
PI3K/AKT/mTOR経路を標的とする治療
- mTOR阻害薬(Rapamycin(Sirolimus)、Everolimusなど)
これらは、TSCやPTEN変異に関連する症候群で用いられることがあり、動物実験ではASD様の行動が改善する効果が報告されています。一方で、免疫抑制、肝毒性、代謝異常などの副作用にも注意が必要です。 - PI3K阻害薬(Idelalisib、Copanlisib、Alpelisibなど)
現時点では主にがん治療で使われており、神経発達障害への応用はまだ研究段階です。 - 翻訳調節関連化合物(4EGI-1など)
タンパク質合成を制御し、EIF4Eの過剰発現やFMR1ノックアウトマウスでの行動異常を改善したという前臨床データがあります。
その他の薬剤
抗うつ薬および抗精神病薬には、ケタミン、アリピプラゾール、パロキセチンなどが含まれます。これらは抑うつや統合失調症の治療に用いられる薬剤であり、一部ではmTORシグナルに作用することで行動への影響を示すことがあります。
天然化合物(フィトセラピューティクス)としては、スルフォラファン、クルクミン、レスベラトロール、ケルセチン、ルテオリンなどが挙げられます。これらの成分はmTOR経路を調整する働きがあることが示されており、動物モデルでは症状の改善が報告されています。
実験的治療(Experimental Therapies)
現在のところ、臨床での使用は確立していませんが、RHEB、ニューロリギン(Neuroligins)、TRIM32などの分子をターゲットとした治療も研究されています。これらは将来的に有望なターゲットとされていますが、現段階ではヒトでの効果や安全性は確認されておらず、慎重な検証が必要です。
予後|Prognosis
自閉スペクトラム症(ASD)および神経発達障害(NDDs)を持つ方の将来的な経過(予後)は、人それぞれで大きく異なります。これは、関与する遺伝子の種類や変異の重症度、診断の時期、受けられる支援の内容など、さまざまな要因に左右されるためです。
予後に影響する要因(Influencing Factors)
予後に影響を与える要因としては、いくつかの点が挙げられます。まず、遺伝子変異の種類や重症度が重要です。重度の変異である場合、発達や生活機能への影響も大きくなる傾向があります。次に、診断の早さと、どれだけ早期に支援が開始されたかも関係します。早く診断され、集中的な介入を受けた方ほど、発達の見通しが良くなることが知られています。また、てんかんや知的障害などの合併症の有無も予後に関わります。これらがある場合は、支援がより複雑かつ長期的になることがあります。さらに、教育的・社会的なサポートの質と量も重要です。安定した支援環境があれば、自立や社会参加への道が広がることが期待されます。
生涯にわたる配慮(Lifelong Considerations)
多くの方は、成人期以降も何らかの支援を必要とすることがあります。ただし、その支援の内容は、年齢や生活環境に応じて変化していきます。PTENやTSC遺伝子に変異がある場合には、悪性腫瘍(がん)を発症するリスクが高いため、定期的な経過観察が望ましいとされています。知的機能や日常生活スキルの改善の可能性については、早期に多方面から支援を受けることで高まることが報告されています。
一方で、適切な支援を受けながら、安定した生活や一定の自立を実現している方も多くおられます。支援の形は人それぞれ異なりますが、それぞれの強みに応じた環境づくりが、生活の質の向上につながると考えられています。
治療に関する課題(Therapeutic Challenges)
mTOR阻害薬や天然成分を用いた治療法(フィトセラピー)に関しては、前向きな研究報告もありますが、ヒトにおける効果は一様ではなく、反応には個人差があるのが実情です。また、脳の部位ごとの違いや、発達のどの時期に治療を開始するか、さらには性別や遺伝的背景といった要因によっても、薬の効果や副作用が異なる可能性があります。
mTOR経路に作用する薬剤を長期間使用する場合には、免疫抑制や肝障害、さらには腫瘍化のリスクなどが懸念されており、使用には慎重な判断が求められます。
このように、予後にはさまざまな不確定要素が存在する一方で、ご本人の持つ可能性を最大限に引き出すためには、早期からの継続的な支援と見守りが非常に重要です。心苦しい情報も含まれますが、ご家族が希望を持ちながら、現実的な準備や選択ができるよう願いを込めてお伝えしています。
引用文献|References
- Nussinov, R., Yavuz, B.R., Arici, M.K. et al. Neurodevelopmental disorders, like cancer, are connected to impaired chromatin remodelers, PI3K/mTOR, and PAK1-regulated MAPK. Biophys Rev 15, 163–181 (2023). https://doi.org/10.1007/s12551-023-01054-9
- Chen, Yan, et al. ‘PI3K-AKT/mTOR Signaling in Psychiatric Disorders: A Valuable Target to Stimulate or Suppress?’ International Journal of Neuropsychopharmacology, vol. 27, no. 2, Feb. 2024, p. pyae010. DOI.org (Crossref), https://doi.org/10.1093/ijnp/pyae010.
- Thomas, Shilu Deepa, et al. ‘mTOR Signaling Disruption and Its Association with the Development of Autism Spectrum Disorder’. Molecules, vol. 28, no. 4, Feb. 2023, p. 1889. DOI.org (Crossref), https://doi.org/10.3390/molecules28041889.
- Baranova, J., Dragunas, G., Botellho, M.C.S. et al. Autism Spectrum Disorder: Signaling Pathways and Prospective Therapeutic Targets. Cell Mol Neurobiol 41, 619–649 (2021). https://doi.org/10.1007/s10571-020-00882-7
やさしい言葉の説明|Helpful Terms
1 自閉スペクトラム症(Autism Spectrum Disorder)|じへいすぺくとらむしょう
生まれつきの脳の発達の違いにより、人との関わりやコミュニケーションが難しい、またはこだわりの強さや感覚の過敏さなどがみられる状態です。症状の出方や強さは人によってさまざまで、早期の理解と支援が重要です。
2 神経発達障害(Neurodevelopmental Disorders)|しんけいはったつしょうがい
脳の発達にかかわるさまざまなプロセスに影響が出る状態です。知的な発達の遅れ、集中しにくさ、言葉の発達の遅れ、運動のぎこちなさなどが含まれます。多くは幼児期に気づかれます。
3 mTOR経路(mTOR pathway)|えむとーあーるけいろ
細胞が栄養状態やエネルギーの量を感知して、成長や働きを調整する仕組みです。脳の発達にも深く関わり、特定の遺伝子の変化がこの経路を過剰に働かせると、神経細胞の接続(シナプス)に異常が起きやすくなることがわかっています。
4 PI3K/AKT経路(PI3K/AKT pathway)|ぴーあいすりーけー/あくとけいろ
細胞が成長や生存のために情報を受け取る主要な信号の流れのひとつです。がんや神経発達に関係する変異がこの経路で報告されています。mTOR経路とつながっています。
5 遺伝子変異(Genetic Mutation)|いでんしへんい
DNAの情報が、親から受け継がれる途中や細胞分裂の過程でわずかに変わることです。すべての変異が問題を起こすわけではありませんが、一部は発達や細胞の働きに影響することがあります。
6 染色体マイクロアレイ(Chromosomal Microarray)|せんしょくたいまいくろあれい
DNAの中にある小さな欠失や重複を検出する検査です。神経発達症の一因となる異常を見つけるのに役立つことがあります。血液などから調べます。
7 全エクソーム解析(Whole-Exome Sequencing)|ぜんえくそーむかいせき
遺伝子の中でもタンパク質を作る部分(エクソン)を中心に詳しく調べる検査です。まれな遺伝子変異の発見に使われることがあります。
8 TSC遺伝子(TSC1/TSC2)|てぃーえすしーいでんし
脳や皮膚などの細胞の成長を調節する遺伝子です。変異があると結節性硬化症(Tuberous Sclerosis Complex)と呼ばれる症候群を起こすことがあり、ASDやてんかんの原因となることもあります。
9 PTEN遺伝子(PTEN gene)|ぴーてんいでんし
細胞の成長やがんの抑制に関わる遺伝子です。変異があると頭囲が大きくなる(巨頭症)ことや、神経の発達、行動の特徴に影響が出ることがあります。
10 クロマチンリモデリング因子(Chromatin Remodeling Factors)|くろまちんりもでりんぐいんし
DNAが巻きついている構造(クロマチン)を緩めたり閉じたりして、遺伝子が必要なときに働くように調整する役割のタンパク質群です。この仕組みがうまく働かないと、発達のタイミングがずれることがあります。