神経伝達の小さな変化が、発達のかたちに影響を与える理由
やさしいまとめ
自閉スペクトラム症(Autism Spectrum Disorder:ASD)は、ことばや視線、感覚の受け取り方など、脳の働きに少し特徴があらわれる神経発達症です。この記事では、ASDの背景に関係していると考えられている「GABA(γ-アミノ酪酸)」という脳内の物質について、やさしく解説します。
GABAは、脳の神経の興奮を落ち着かせ、情報をスムーズに伝える働きがあります。子どもの脳の発達の途中では、一時的にGABAが反対に興奮を助けることがあり、その切り替えがうまくいかないと、ASDのような特性があらわれやすくなると考えられています。遺伝的な背景(例:SLC12A5, MECP2など)や脳内のイオンバランスも深く関係しています。
この記事では、ASDに関係するしくみ、よく見られる症状、検査や診断の方法、治療や支援の可能性、そして将来の見通しについて、できるだけわかりやすくご紹介しています。お子さまやご家族の理解と支援のヒントになれば幸いです。
概要|Overview
GABA(ガンマアミノ酪酸:γ-aminobutyric acid)は、成熟した哺乳類の脳において主要な「抑制性神経伝達物質」として広く知られています。神経細胞の活動を落ち着かせる働きがあり、脳の回路が正しく形成され、情報が適切に伝わるようにするために重要な役割を担っています。
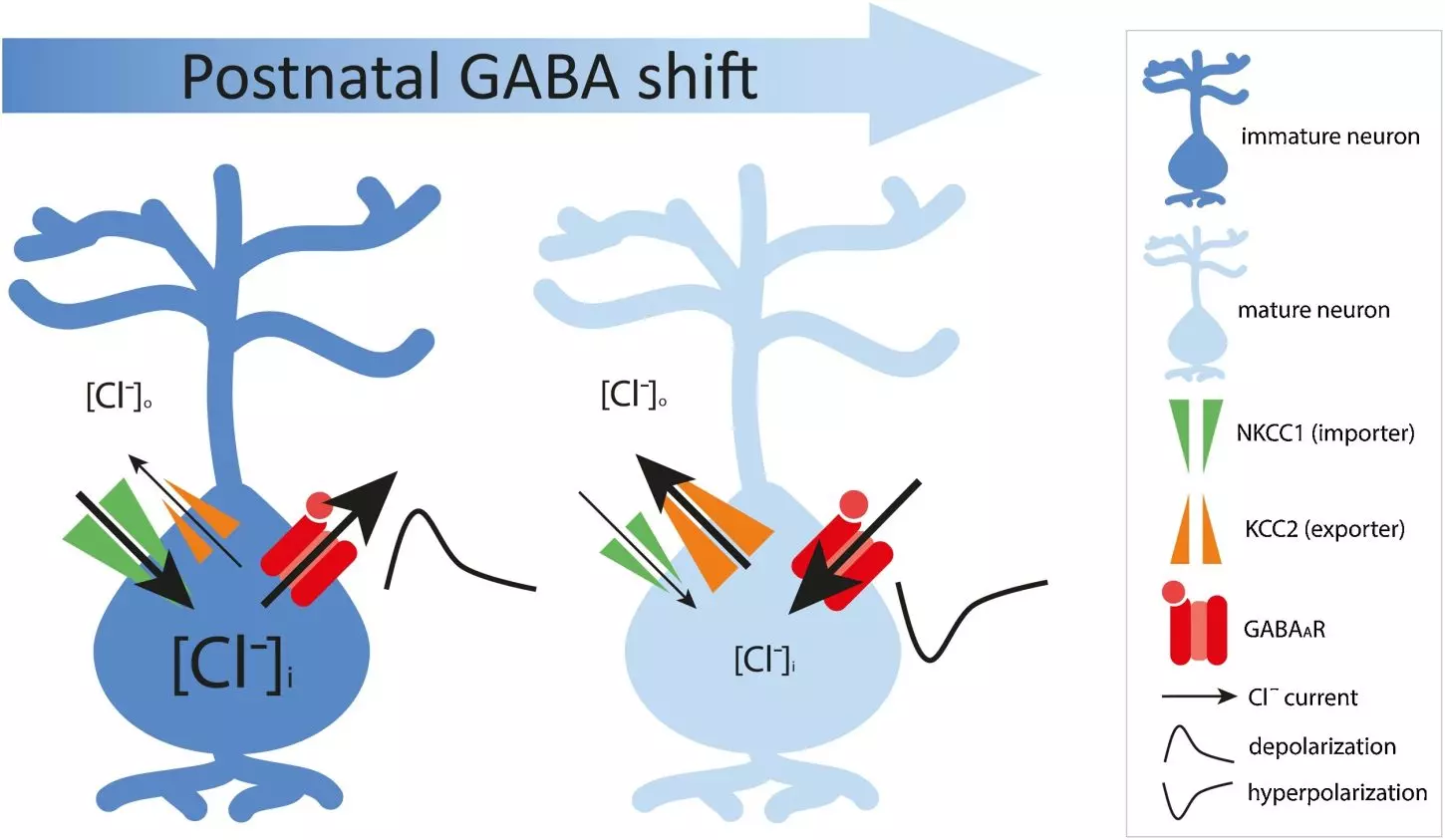
生後間もない時期の脳では、GABAによる信号は一時的に「興奮性(depolarizing)」として働きます。これは、神経細胞の中に塩化物イオン(Cl⁻)が多く存在しているためであり、NKCC1という塩化物イオン輸入タンパク質の働きによってこの状態が保たれています。
その後、脳の成長に伴ってKCC2という塩化物イオンを外へ排出するタンパク質(塩化物輸出体)が増えてくると、GABAの働きは「抑制性(hyperpolarizing)」に切り替わります。この切り替わりは「生後のGABAシフト(postnatal GABA shift)」と呼ばれ、神経回路の発達において極めて重要な過程です。
このGABAシフトは単なる化学変化ではなく、神経細胞の増殖や分化、移動、シナプスの形成や刈り込み、そして神経ネットワーク全体のリズム(ネットワーク振動)や、興奮と抑制のバランス(excitation/inhibition balance, E/Iバランス)など、脳のあらゆる発達段階に深く関わっています。
この切り替わりのタイミングや場所、程度がうまくいかない場合には、自閉スペクトラム症(Autism Spectrum Disorder, ASD)をはじめとしたさまざまな神経発達症(Neurodevelopmental Disorders, NDDs)と関連することが報告されています。
実際、ASDのモデル動物や患者の研究においては、GABAの働きが不足している場合だけでなく、逆に過剰に働いているケースも確認されています。こうした異常は、GABA受容体(GABA receptors)や塩化物輸送体、シグナル調節因子を含む遺伝子の変異に関連しています。
さらに重要なのは、これらのGABA関連の異常が、神経細胞の成長や代謝、可塑性(柔軟に変化する力)を司る「PI3K–AKT–mTOR経路(pathway)」と深く交差していることです。この経路の異常もまた、ASDなどの発症メカニズムに影響を与える要因と考えられています。
遺伝子領域|Implicated Genomic Region
GABAの働きに関する異常は、さまざまな遺伝子領域に起因していることが知られています。こうした遺伝子は、GABA受容体の構成要素、塩化物の輸送に関わる共輸送体、シナプス関連タンパク質、転写因子などをコードしています。
たとえば、15q11–q13領域はASDにおいてしばしば「重複(duplication)」が見られる領域であり、GABRB3, GABRA5, GABRG3といったGABA<sub>A</sub>受容体のサブユニットをコードする遺伝子が含まれています。また、UBE3Aというシナプス形成を調整する遺伝子もこの領域に存在しており、「Dup15q症候群(Dup15q syndrome)」と呼ばれるASDの一形態に関連しています。
さらに、GABAの極性(興奮性から抑制性への変化)を決定づける主要な塩化物共輸送体であるKCC2(SLC12A5)とNKCC1(SLC12A2)も重要です。これらの遺伝子における変異や発現の異常は、GABAの働きが抑制に切り替わるはずの時期に引き続き興奮性のままであるといった現象を引き起こし、神経回路の過剰な興奮や異常な発達につながることがあります。
GABA経路と相互に作用するもう一つの重要な分子経路が、PI3K–AKT–mTOR経路です。PTEN, TSC1, TSC2, NF1などの遺伝子はこの経路に関与しており、神経の興奮性やタンパク質合成の調整、塩化物輸送体の発現を制御する働きがあります。
そのほか、ASDに関与することが知られているMECP2, FMR1, SHANK1/2/3, CNTNAP2/3/4, CDKL5といった遺伝子も、GABA性シナプスの形成や抑制性介在ニューロン(interneuron)の働き、E/Iバランスの維持に関係しています。
さらに補足すると、GABAの合成に関わるGAD1/2(グルタミン酸脱炭酸酵素をコード)、シナプス構造を安定化させるGPHN(ギファリン)、シナプス接着分子であるNRXN1–3(ニューレキシン)やニューロリギン2なども、GABA受容体の局在と安定に深く関与しています。
これらの遺伝的要因は単独で発症を決定づけるわけではなく、多くの場合、エピジェネティックな要素(遺伝子の働きを調整する仕組み)や環境因子、性差などと相互に影響し合っています。特に、BDNF(脳由来神経栄養因子)とその受容体TrkBによるKCC2の調節は、実験モデルだけでなく臨床研究においても繰り返し注目されている重要なメカニズムです。
疾患名|Disorder
GABAの働きに異常があるとされる代表的な疾患は、「自閉スペクトラム症(Autism Spectrum Disorder:ASD)」です。ASDは非常に多様性のある神経発達症の一つで、人によって現れる特性や困りごとの形はさまざまです。
この疾患では、言葉や表情、身振りを使った「社会的なやりとり」に困難が見られたり、自分の興味に強くこだわる傾向や、特定の行動を繰り返す様子が特徴として現れます。
ASDをもつ方の多くは、てんかん(epilepsy)や知的発達の遅れ(知的障害)、注意欠如・多動症(ADHD)、睡眠障害、感覚の過敏さといった「併存する症状(comorbidities)」を経験されることもあります。これらはいずれも、脳の「興奮と抑制のバランス(E/Iバランス)」がうまく保てていないことと関係があると考えられています。
GABAの働きの異常は、このバランスの乱れに直接関与しており、原因にもなれば、結果としても現れることがあると報告されています。つまり、もともとGABAの異常が脳の発達に影響を与え、それがASDの特性として現れることもあれば、他の遺伝子や環境の影響で脳に変化が生じた結果として、GABAの働きが後から乱れることもある、ということです。
特に以下のような、特定の遺伝子変異や染色体の変化によって起こる「症候性ASD(syndromic autism)」では、GABAの回路に関する異常が共通して見られています:
- レット症候群(Rett syndrome):MECP2遺伝子の変異による疾患で、主に女児に多く見られます。
- 脆弱X症候群(Fragile X syndrome):FMR1遺伝子の機能低下による知的障害を伴うASDの一形態です。
- アンジェルマン症候群(Angelman syndrome):UBE3A遺伝子の異常によるもので、重度の発達障害を伴います。
- CDKL5欠損症候群(CDKL5 deficiency disorder):てんかんや重度の神経発達遅滞を伴うまれな疾患です。
- Dup15q症候群(Duplication 15q syndrome):GABA受容体関連遺伝子の重複によって生じ、ASD様の特性が現れます。
- ダウン症候群(Down syndrome):21番染色体の重複による先天性疾患で、NKCC1の発現異常などが報告されています。
- ドラベ症候群(Dravet syndrome):SCN1A遺伝子の変異により、GABA抑制性ニューロンの機能が障害されるてんかん症候群です。
これらの症候群に共通するのは、GABAを中心とした神経回路の機能障害、塩化物イオンの恒常性の乱れ(chloride homeostasis disruption)、そして脳の過剰な興奮(network hyperexcitability)です。また、それぞれの症状の背景には、PI3K–AKT–mTOR経路やその他の発達関連シグナル経路が関与していることがわかってきています。
疫学|Epidemiology
自閉スペクトラム症(ASD)は、現在、世界中でもっともよく見られる神経発達症のひとつであり、統計的には、おおよそ36人に1人の子どもが診断を受けていると報告されています。
また、ASDには明確な性差があり、診断される割合は男性のほうが3〜4倍ほど多いとされています。この理由はまだ完全には解明されていませんが、GABAの機能や塩化物輸送体の発現タイミングに性差があることが、一因として考えられています。たとえば、女児ではGABAの「抑制性」への切り替わりが男児よりも早いという研究も報告されています。
ASDの方のうち、およそ20〜30%がてんかんを併発することも知られています。これは、脳の「興奮と抑制のバランス(E/Iバランス)」がうまく保てていないことを反映している可能性があります。
そのほかにも、知的障害、注意欠如・多動症(ADHD)、睡眠障害、感覚過敏など、GABAの機能異常と関連するさまざまな症状が、しばしば併存することが確認されています。
また、ASDの中には、まれではありますが、単一遺伝子や染色体異常が明らかになっている「症候性ASD」も存在します。これらは個々に異なる遺伝的背景を持ちつつも、GABA経路の機能不全や塩化物恒常性の乱れといった共通のメカニズムを通じて発症していることが多く、分子レベルでの理解を深めるうえで重要な手がかりとなっています(詳細は前章の「疾患名|Disorder」をご参照ください)。
病因|Etiology
自閉スペクトラム症(ASD)やそれに関連する神経発達症(Neurodevelopmental Disorders:NDDs)の原因は、非常に多様であり、ひとつの要因に限定されるものではありません。遺伝子の変異や環境的な影響、さらには脳の回路や細胞の働き方など、さまざまなレベルでの要素が重なり合って関係していることが、現在の研究で明らかになっています。
その中でも特に注目されているのが、GABAの働きの異常と、塩化物イオンの恒常性(chloride homeostasis)の乱れです。これらは多くの症例に共通してみられる重要なメカニズムであり、大きく2つの軸から説明されます。
1 塩化物輸送体のアンバランスとGABAの極性変化の失敗
胎児期から生後まもない時期の脳では、GABAは本来「興奮性(depolarizing)」に働いて、神経細胞の成長や移動を促す役割を果たします。この時期、神経細胞の中にはCl⁻(塩化物イオン)が多く存在し、NKCC1(SLC12A2)という塩化物の輸入体が活発に働いています。
その後、発達が進むと、KCC2(SLC12A5)という塩化物の輸出体の働きが強まり、細胞内のCl⁻濃度が下がることで、GABAは「抑制性(hyperpolarizing)」に切り替わります。このタイミングの変化こそが、神経回路の成熟や感覚処理、行動制御にとって非常に重要な転換点となります。
しかし、この「GABAの極性シフト(polarity shift)」が何らかの理由で遅れる、あるいは起こらないと、GABAが本来抑えるべき神経活動を逆に高めてしまい、回路の過剰な興奮や誤った接続が生じることになります。これにより、ASDに見られるような行動的特徴や感覚の過敏さなどが引き起こされる可能性があります。
また、逆に早すぎるGABAの抑制化(KCC2の過剰発現やNKCC1の早期消失)が起こると、神経細胞の正しい位置への移動(ニューロンの移動)や回路の可塑性が損なわれることがあります。こうした異常は、レット症候群、脆弱X症候群、CDKL5欠損症候群、環境要因によるASDモデル(妊娠中の炎症やバルプロ酸への曝露など)で繰り返し観察されています。
2 GABA経路およびmTOR経路における遺伝的・分子的異常
ASDに関連する多くのリスク遺伝子は、GABAの働きに関与する構造や調節機能に関わっています。たとえば:
- GABA受容体のサブユニット:GABRB3, GABRA5, GABRG3
- GABA合成関連酵素や輸送体:GAD1/2(グルタミン酸脱炭酸酵素)、VGAT(GABA輸送体)、gephyrin(受容体安定化)
- 塩化物輸送体:KCC2(SLC12A5)、NKCC1(SLC12A2)
- シナプス接着分子:NRXN1–3(ニューレキシン)、ニューロリギン(NLGN2など)
- 転写調節因子:MECP2、TCF4、CHD8
さらに重要なのは、これらのGABA関連遺伝子の多くが、PI3K–AKT–mTOR経路とも深く関わっている点です。
- PTEN、TSC1/2、NF1といった遺伝子は、mTOR経路の抑制因子として働きます。これらに変異があると、タンパク質合成が過剰になり、シナプスの調節が乱れることがあります。
- SHANK3、UBE3A、CHD8などの遺伝子は、GABA性シナプスの構造や数の調整、さらにはmTOR経路の活性化にも関与しています。
- MECP2(レット症候群の原因遺伝子)は、BDNF–TrkB経路を介してKCC2の発現を調整し、GABAの極性変化に影響を与えます。
さらに、バルプロ酸の胎児期曝露、母体の炎症、酸化ストレスなどの環境因子も、塩化物輸送体やミクログリア(脳内免疫細胞)を通じてGABAの発達に影響を及ぼすことがわかっています。
このように、GABAの働きの異常は、一次的な遺伝的要因によって直接引き起こされる場合と、他の神経ネットワークの異常に伴って二次的に生じる場合の両方があります。特に、PI3K–AKT–mTOR経路の過剰な活性化が、GABAの働きを抑えたり、神経回路の可塑性を損なったりすることが報告されています。
症状|Symptoms
GABAの働きが、脳の発達の重要な時期において乱れてしまうと、自閉スペクトラム症(ASD)やその他の神経発達症に共通するさまざまな症状が現れることがあります。これらの症状は、単に個々の神経細胞の問題だけでなく、脳全体のネットワーク機能やリズム(脳波活動)、可塑性(柔軟に変化する力)の異常を反映しています。
主な行動的特徴
- 社会的なやりとりの困難
前頭葉や側頭葉などの脳領域でE/Iバランスが崩れていると考えられており、とくにPV+介在ニューロンの働きが弱まると、社会的な情報の処理に必要な脳の同期性が損なわれることがあります。 - 特定の関心への強いこだわりや繰り返し行動
GABA-A受容体やその輸送体に異常がある動物モデルでも同様の行動が見られることが報告されています。 - 感覚過敏(とくに触覚や聴覚)
GABAが視床–大脳皮質の入力を調整する働きに影響があると、刺激の強さをうまく制御できなくなることがあります。
神経学的な併存症
- てんかんやけいれん発作
GABAがいつまでも興奮性のままであると、Cl⁻を排出できず神経が過剰に興奮し、発作を引き起こす原因になることがあります(例:ドラベ症候群、レット症候群)。 - 知的障害
GABAが正常に機能しないと、回路の洗練(シナプスの刈り込み)やネットワーク形成に支障をきたし、学習や記憶に関わる機能が十分に発達しないことがあります。 - 睡眠障害
GABAの働きが視床下部や脳幹で乱れると、体内時計や睡眠のリズムに影響が出る可能性があります。
神経生理学的な特徴
- ガンマ波(30–80 Hz)の減少
PV+介在ニューロンの働きが弱まると、ガンマ波と呼ばれる脳の高周波活動が減少し、情報の処理効率が低下すると考えられています。 - GABA極性シフトの遅れや乱れ
神経ネットワークの同期性が失われ、「巨大脱分極電位(GDPs)」と呼ばれる異常な活動が持続することがあります。 - 脳波(EEG)パターンの異常
スペクトルのばらつきが大きく、ガンマ帯域の整合性が低下する傾向がASDの人々にみられます。
性別および部位ごとの特徴
- 女児の方がGABAの切り替わりが早い
このことが、ASDの性差に一部影響している可能性があります。 - 脳部位による違い
GABA関連マーカーや塩化物輸送体の異常は、前部帯状皮質(anterior cingulate cortex)、海馬(hippocampus)、視覚皮質(visual cortex)など、脳の部位によって異なる様相を呈します。
このように、GABAの異常に関連する症状は、発達のタイミングのズレと、脳の部位ごとの脆弱性の組み合わせから生じていると考えられています。回路レベルでの「抑制の欠如(disinhibition)」が、こうした多様な症状の根本にある病態の中心と位置づけられています。
検査・診断|Testing & Diagnosis
自閉スペクトラム症(Autism Spectrum Disorder:ASD)の診断は、現在も主に臨床的な観察と行動評価に基づいて行われています。国際的には、「DSM-5(精神障害の診断と統計マニュアル第5版)」の診断基準に従い、社会的なコミュニケーションの持続的な困難や、限定的で反復的な行動や興味といった特徴の有無を確認します。
しかし、近年の研究では、ASDの背景にある生物学的な多様性をより深く理解し、将来的な個別化医療(precision medicine)につなげるため、バイオマーカーを用いた層別化(stratification)の可能性が注目されています。
脳画像・神経生理学的なバイオマーカー
- 磁気共鳴分光法(Magnetic Resonance Spectroscopy:MRS)
この非侵襲的な検査では、脳内のGABA濃度を特定の領域で定量的に測定することができます。ASDの研究では、前部帯状皮質(anterior cingulate cortex)や前頭葉皮質、体性感覚領域などにおいて、GABAとグルタミン酸の比率(GABA/glutamate比)が低下していることが報告されています。ただし、年齢や個人差によって結果にはばらつきがあります。 - 脳波検査(Electroencephalography:EEG)
EEGでは、ASDの方においてガンマ波(30〜80Hz)の振幅低下やスペクトルの傾き(spectral slope)の異常、E/Iバランスの変動性増大といったパターンが報告されています。これらの指標は、GABAの働きに関連する神経活動のバイオマーカーとして、今後の分類や治療効果の予測に役立つ可能性があります。 - 両眼視野競合パラダイム(Binocular Rivalry Paradigm)
視覚の情報処理におけるGABA濃度と知覚の切り替わり速度との相関が崩れることが観察されており、視覚野におけるGABAの抑制機能の乱れが示唆されています。
解剖学的および遺伝的な所見
ASDに関連する神経回路の異常については、剖検脳組織の研究からも重要な手がかりが得られています。特に、パルブアルブミン陽性(PV+)介在ニューロンの減少、GABA合成酵素GAD65/67の低下、ならびに塩化物輸出体KCC2やGABA受容体遺伝子のエピジェネティックな発現抑制などが報告されており、抑制性神経伝達の低下と関連づけられています。
一方で、ASDの診断において遺伝子検査が標準的に行われるわけではないものの、個別の症例では遺伝的要因が明らかになることがあります。具体的には:
- MECP2、FMR1、SHANK3などの単一遺伝子変異
- GABA関連遺伝子(例:GABRB3、GABRA5、SLC12A5)に見られる一塩基多型(SNPs)
- Dup15q症候群などに代表される染色体構造の変化(コピー数変異:CNVs)
こうした所見は、症候性ASDの診断補助や、将来的な個別化治療の選択肢を考える上で有用な情報となる可能性があります。
治療法と管理|Treatment & Management
現時点で、自閉スペクトラム症(ASD)に対する治療薬は限られており、主に併存する症状(いらだち、てんかん、睡眠障害など)への対処が中心です。
しかし、近年はGABAの機能異常や塩化物恒常性の乱れに着目し、それらを正すことを目指した治療法の研究が進められています。これらは、動物実験から臨床試験段階にあるものまでさまざまですが、以下のようなアプローチが挙げられます。
1 塩化物輸送体を標的とする治療
ブメタニド(Bumetanide)
ブメタニドは、NKCC1(ナトリウム・カリウム・塩化物共輸送体1)と呼ばれる塩化物の輸入体を選択的に抑制する利尿薬です。この薬剤を使用することで、神経細胞内の塩化物イオン(Cl⁻)の濃度を低下させる作用が期待されており、それによってGABA(γ-アミノ酪酸)の働きを「脱分極性(興奮性)」から「過分極性(抑制性)」へと導く効果が示唆されています。
動物実験では、ASD(自閉スペクトラム症)モデルマウスを対象に、行動面および神経ネットワークのレベルで改善が見られたとの報告があります。
また、小規模ながら人を対象とした臨床試験でも、一部の小児患者においてASD関連症状の改善が確認されています。特に、脳波(EEG)に異常所見があるケースや、炎症性サイトカインの値が高い子どもにおいて、効果が現れやすい傾向があるとされています。
一方で、ブメタニドの使用にはいくつかの課題もあります。まず、血液脳関門(BBB)を通過する力が弱く、脳内への到達が限定的であることが挙げられます。また、副作用としては、低カリウム血症(血中カリウム濃度の低下)や脱水といった体液バランスの異常が生じる可能性があるため、慎重なモニタリングが必要です。
KCC2活性化薬
まだ前臨床段階ですが、KCC2の機能を高めてCl⁻の排出を促進する薬剤(例:CLP257など)が開発されています。これにより、GABAの抑制作用を回復させ、シナプスの可塑性や樹状突起スパインの構造を正常化する可能性が示唆されています。
2 GABA受容体を調整する薬剤
GABA-A受容体作動薬・モジュレーター
GABA-A受容体作動薬やモジュレーターには、ガボキサドールやベンゾジアゼピン系薬などが含まれます。これらの薬剤は、神経の活動を抑える働きを持つGABAの「持続的な抑制作用(トニック抑制)」を高めることが可能とされています。
ただし、その効果には個人差があることが知られています。たとえば、ある方では眠気が強く出る一方で、別の方では逆に興奮や不安の悪化を引き起こすケースも報告されています。
GABA-B受容体作動薬(例:バクロフェン)
動物モデルでは、反復行動の減少や脳波の正常化が報告されており、今後の可能性が期待されています。
3 分子経路を標的とした治療
PI3K–AKT–mTOR経路の調整
結節性硬化症(tuberous sclerosis)やPTEN異常を伴うASDでは、ラパマイシン誘導体(例:エベロリムス)によってE/Iバランスやネットワークの同期性が改善されるという報告があります。
BDNF–TrkB経路の調整
この経路を刺激することで、KCC2の発現を正常化させ、GABAの極性シフトを促進する治療戦略も提案されています。
4 遺伝子および細胞治療
遺伝子治療の分野では、レット症候群モデルにおいて、MECP2遺伝子を再活性化することにより、GABAの伝達機能および行動面の一部が回復したという結果が報告されています。
また、細胞治療に関しては、胚発生時の中脳腹側領域(MGE)由来の介在ニューロンを移植する実験において、ASDモデルマウスの神経抑制機能および社会的行動が回復したという報告もあります。
5 非薬物的な介入
感覚刺激の強化(sensory enrichment)については、齧歯類モデルを用いた研究において、環境からの刺激を与えることでKCC2の発現が促進され、抑制性の神経機能が回復することが示されています。
また、食事制限や運動療法、さらにtDCS(経頭蓋直流刺激)やTMS(経頭蓋磁気刺激)などの神経刺激法については、GABAのトーンを調整する可能性がある方法として、現在も研究が進められている段階です。
今後の展望
今後の研究と臨床応用においては、いくつかの取り組みが注目されています。たとえば、EEG(脳波)ガンマ波やサイトカインプロファイルを用いて、治療効果の予測や患者層の分類(層別化)を行う試みが進められています。
また、薬物療法と非薬物療法の併用による相乗的な効果を目指した介入も検討されています。
さらに、iPS細胞由来の疾患モデルを用いた個別化薬剤スクリーニングも研究が進んでおり、将来的にはより精密な治療選択につながる可能性があります。
予後|Prognosis
自閉スペクトラム症(ASD)を持つ方の将来の見通し(予後)は、非常に幅が広く、GABAの働きや神経回路全体の機能異常がいつ、どのように起こるかによって、大きく左右されます。
より良い予後と関連する要因
- GABAの極性変化(抑制への切り替え)が起こる重要な時期に、早期から適切な支援が行われた場合、神経回路の発達が促進され、長期的な機能の改善が期待できます。
- 知的障害や言語発達の大きな遅れがない場合、社会的スキルや適応力が高まりやすい傾向があります。
- 原因となる遺伝子変異が特定されている場合、たとえばKCC2/NKCC1のアンバランスが確認されたお子さんには、ブメタニドなどの治療法が選択肢となる可能性があります。
困難が続く場合に関連する要因
- GABAの極性変化が大きく遅れる、または起こらない場合、脳の回路構造に恒久的なずれ(誤配線)が生じることがあり、皮質の可塑性も低下します。
- GABAが興奮性のままであることによるてんかん(例:レット症候群、ドラベ症候群)は、より重度な症状と関連しやすいとされています。
- 思春期以降のホルモン変化、環境ストレス、慢性炎症などによって、GABA系の機能は成人期にも変化を受ける可能性があり、注意深い見守りが必要です。
発達の可塑性と代償の力
とはいえ、GABA系の初期の不調があったとしても、脳は本来、回復力と適応力(可塑性)を持っています。経験を通じて新たな回路を作り出したり、別の方法で機能を補う力を持っているのです。
実際、多くの方が、早期のGABA異常があっても、別の神経経路を使って学習し、社会的なやりとりを身につけ、日常生活に適応していくことが報告されています。こうした回復の可能性は、適切な支援と環境の整備によって大きく高まると考えられています。
結語|Conclusion
GABAという一つの神経伝達物質の仕組みを深く理解することは、ASDのような複雑な神経発達症の背後にあるメカニズムを明らかにする鍵となります。それと同時に、私たちの脳がどれほど精密に作られ、どれほど多くの要素が奇跡のようなバランスで保たれているかを、あらためて感じさせられます。
GABA受容体や塩化物共輸送体、PI3K–AKT–mTOR経路など、さまざまな分子が互いに連携しながら、興奮と抑制のバランスを静かに支えています。しかし、そのバランスは、ほんのわずかなタイミングのずれや遺伝子の変異、あるいは一時的な炎症反応によって崩れることがあります。
こうした研究から見えてきたのは、「決して避けられない運命」ではなく、脆さと回復力のせめぎあいです。GABAが興奮性のままで残ってしまうときも、介在ニューロンの移動がうまくいかないときも、脳は何とかして新しい経路を探し、少しずつ順応しようとします。
この事実は、科学的な意味だけでなく、私たち一人ひとりに対する大切な問いかけでもあります。人が“機能している”ように見えるからといって、本当に困っていないとは限りません。
そして、支援の必要性は、外から見える“症状の重さ”だけで決まるものではないということを、私たちは深く理解しておく必要があります。
この複雑で、壊れやすく、しかし驚くほどしなやかな神経系が、日々どのように働いているのか。そして、そのなかで、人が感じ、学び、愛し、意味を見出していくということ自体が、すでに驚くべき営みです。バランスが少し崩れていたとしても、それは「可能性が失われた」ということではありません。人の発達は、はかなく、しかし尊く、豊かなものです。
そのすべての瞬間が、支援と理解に値する価値を持っていることを、どうか忘れないでください。
引用文献|References
- Topchiy, Irina, et al. ‘GABA System as the Cause and Effect in Early Development’. Neuroscience & Biobehavioral Reviews, vol. 161, Jun. 2024, p. 105651. DOI.org (Crossref), https://doi.org/10.1016/j.neubiorev.2024.105651.
- Bruni, Oliviero, et al. ‘Herbal Remedies and Their Possible Effect on the GABAergic System and Sleep’. Nutrients, vol. 13, no. 2, Feb. 2021, p. 530. DOI.org (Crossref), https://doi.org/10.3390/nu13020530.
- Tang, X., Jaenisch, R. & Sur, M. The role of GABAergic signalling in neurodevelopmental disorders. Nat Rev Neurosci 22, 290–307 (2021). https://doi.org/10.1038/s41583-021-00443-x
- Zhao, Haisheng, et al. ‘GABAergic System Dysfunction in Autism Spectrum Disorders’. Frontiers in Cell and Developmental Biology, vol. 9, Feb. 2022, p. 781327. DOI.org (Crossref), https://doi.org/10.3389/fcell.2021.781327.
- Cherubini, Enrico, et al. ‘Dysregulation of GABAergic Signaling in Neurodevelomental[sic] Disorders: Targeting Cation-Chloride Co-Transporters to Re-Establish a Proper E/I Balance’. Frontiers in Cellular Neuroscience, vol. 15, Jan. 2022, p. 813441. DOI.org (Crossref), https://doi.org/10.3389/fncel.2021.813441.
- Ferranti, Anthony S., et al. ‘Novel Pharmacological Targets for GABAergic Dysfunction in ADHD’. Neuropharmacology, vol. 249, May 2024, p. 109897. DOI.org (Crossref), https://doi.org/10.1016/j.neuropharm.2024.109897.
- Giniatullin, Rashid, and Enrico Cherubini. ‘Gabaergic Signalling in Autism Spectrum Disorders (ASD): Role of Glial Cells and Therapeutic Perspectives’. Brain, Behavior, and Immunity, vol. 129, Oct. 2025, pp. 681–89. DOI.org (Crossref), https://doi.org/10.1016/j.bbi.2025.07.003.
- Peerboom, Carlijn, and Corette J. Wierenga. ‘The Postnatal GABA Shift: A Developmental Perspective’. Neuroscience & Biobehavioral Reviews, vol. 124, May 2021, pp. 179–92. DOI.org (Crossref), https://doi.org/10.1016/j.neubiorev.2021.01.024.
やさしい言葉の説明|Helpful Terms
1 自閉スペクトラム症(Autism Spectrum Disorder, ASD)|じへいすぺくとらむしょう
神経の発達の仕方に特徴があり、社会的なやりとりや感覚の受け取り方、興味や行動のパターンに違いがあらわれる状態です。症状の出方や強さには個人差が大きく、知的能力や会話の力に幅があります。
2 神経発達症(Neurodevelopmental Disorder)|しんけいはったつしょう
脳の発達の過程に関わる症状の総称で、自閉スペクトラム症、注意欠如・多動症(ADHD)、知的発達症などが含まれます。遺伝や環境など、さまざまな要因が重なって起こると考えられています。
3 GABA(Gamma-Amino Butyric Acid, γ-アミノ酪酸)|がば(がんまあみのらくさん)
脳内で神経の働きを落ち着かせる役割をもつ物質(抑制性神経伝達物質)です。子どもの発達中は一時的に神経を活性化する働きもありますが、成長に伴い神経の興奮を抑える役割に切り替わります。
4 抑制性神経伝達物質(Inhibitory Neurotransmitter)|よくせいせいしんけいでんたつぶっしつ
脳内で神経の活動を静かにする働きを持つ化学物質です。GABAが代表的で、神経の過剰な興奮を防ぎ、脳のバランスを保つのに重要です。
5 興奮と抑制のバランス(Excitation/Inhibition Balance, E/Iバランス)|こうふんとよくせいのばらんす
脳内で「神経が活発に働く力」と「それを落ち着かせる力」のバランスを指します。このバランスが崩れると、感覚が過敏になる、睡眠が乱れる、けいれんが起きやすくなるといった症状につながることがあります。
6 GABAの極性シフト(GABA Polarity Shift)|がばのきょくせいしふと
GABAの働きが発達に伴って「興奮性」から「抑制性」へと変化する現象です。このタイミングが遅れたり、うまくいかなかったりすると、神経回路の形成に影響し、発達に特徴が出る場合があります。
7 塩化物輸送体(Chloride Transporter)|えんかぶつゆそうたい
神経細胞内の塩化物イオン(Cl⁻)の出入りを調整するたんぱく質です。KCC2はCl⁻を外へ出し、NKCC1は取り込む働きを持ちます。GABAの働きの転換(極性シフト)に深く関わっています。
8 KCC2(SLC12A5)|けーしーしーつー
塩化物イオンを神経細胞の外へ排出する輸送体です。発達が進むと増加し、GABAが抑制性に切り替わるために必要です。
9 NKCC1(SLC12A2)|えぬけーしーしーわん
塩化物イオンを神経細胞内に取り込む輸送体で、胎児期や乳児期に多く見られます。この働きにより、GABAが一時的に興奮性になることがあります。
 中文
中文