やさしいまとめ
自閉スペクトラム症(Autism Spectrum Disorder:ASD)は、ことばの発達の遅れや社会的なやりとりのむずかしさ、くり返しの行動などが特徴の神経発達症です。近年の研究では、こうした発達の特性に、脳内の情報伝達を担う「Wnt/β-カテニン経路(カノニカルWntシグナル)」の異常が関係していることが注目されています。
この経路は、胎児期の脳の発達に深く関わっており、神経細胞の成長やつながりを調整しています。Wntシグナルの働きが過剰または低下すると、脳の構造や神経回路のバランスが崩れ、ASDのさまざまな症状に関連することがわかってきました。特に、CHD8、CTNNB1、WNT2、TCF7L2などの遺伝子の異常は、神経細胞の増殖やシナプスの形成異常と関係しているとされています。
本記事では、Wnt/β-カテニン経路がどのようにASDと関係しているのか、症状、関連する遺伝子、検査、そして将来の治療の可能性について、専門的な内容をやさしく解説しています。お子さまの発達にご不安をお持ちの方や、ASDについてより深く知りたい方に向けて、最新の研究に基づいた安心できる情報をお届けします。
概要と背景|Overview & Background
自閉スペクトラム症(Autism Spectrum Disorder:ASD)は、社会的コミュニケーションの困難さや反復的な行動、興味のかたよりを特徴とする神経発達症であり、遺伝的背景や発達中の神経回路形成の異常が複雑に関与しています。ASDは多因子性かつ多遺伝子性(polygenic)な疾患であり、その表現型の多様性から、従来は「異質性の高い症候群」として捉えられてきました。
しかし近年、ASDに関連する複数の遺伝的要因が、共通してカノニカルWnt/β-カテニン経路(canonical Wnt/β-catenin signaling pathway)に関与していることが示されつつあります。この経路は中枢神経系(CNS)の発達において、以下のようなプロセスを調節しています:
- 神経前駆細胞(neural progenitor cells)の増殖と分化
- 神経細胞の移動、および大脳皮質の層構造形成(皮質ラミネーション)
- シナプスの形成と樹状突起スパインの成長
- 神経回路の可塑性(柔軟な変化)と安定性の維持
ASD患者およびモデル動物において、Wnt経路の異常は大脳皮質の過形成(大頭症)、シナプス形成異常、神経回路の接続性の変化など、神経発達のさまざまな側面に影響を及ぼすことが報告されています。
多くの研究で、Wntシグナル経路の異常がASDの病態に関与している可能性が示されていますが、すべてのASDの方に同じような変化が見られるわけではなく、因果関係については現在も研究が進められている段階です。ASDには、Wnt経路以外にも多くの分子経路が関わっていることが知られていますが、本記事では、そうした複雑な背景の中から、本記事では、Wntシグナルというひとつの視点からASDを見つめ直し、理解を深めるための小さな手がかりとなることを願ってご紹介しています。
Wnt/β-カテニン経路の分子機構|Wnt/β-Catenin Signaling Mechanism
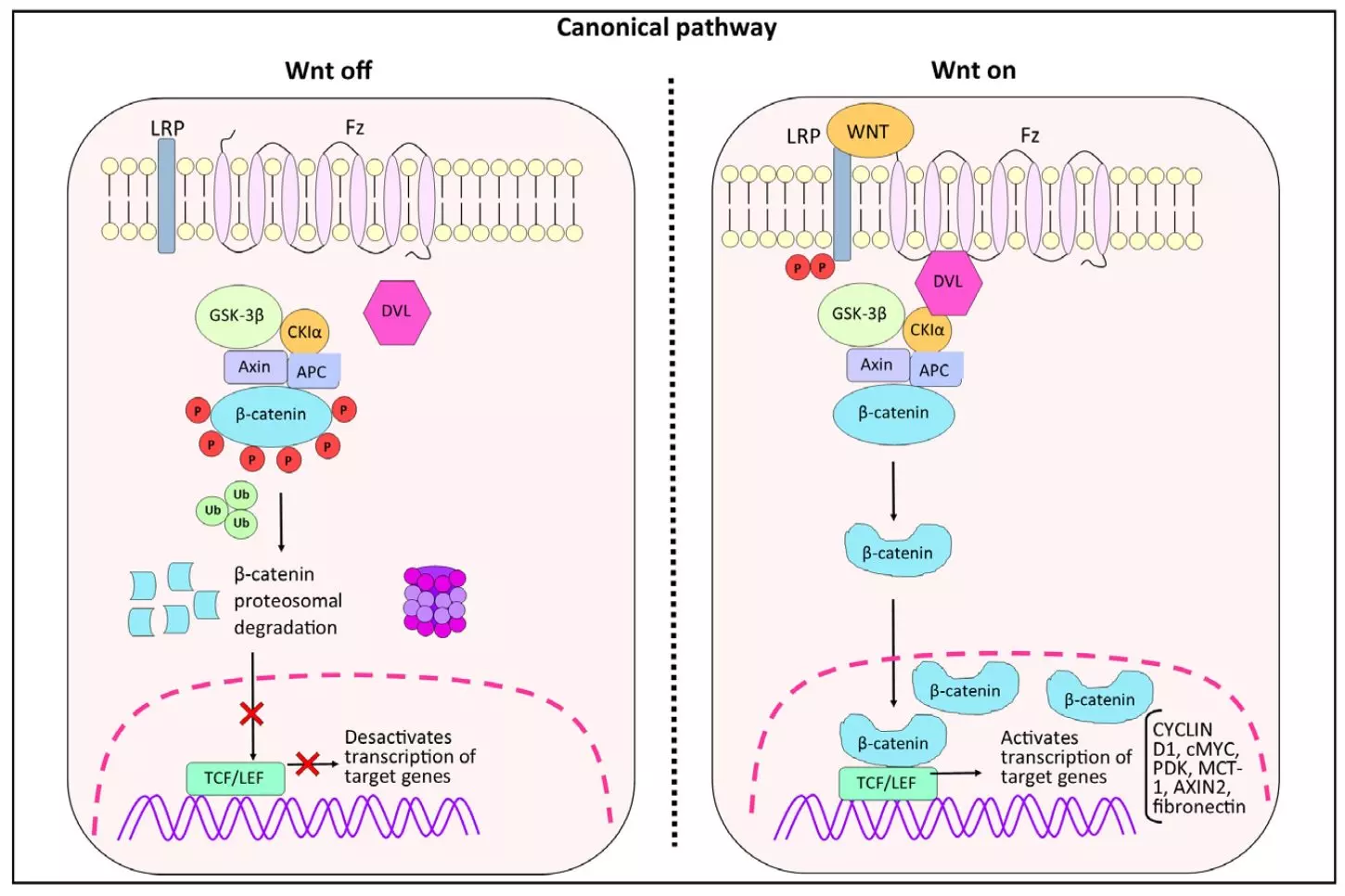
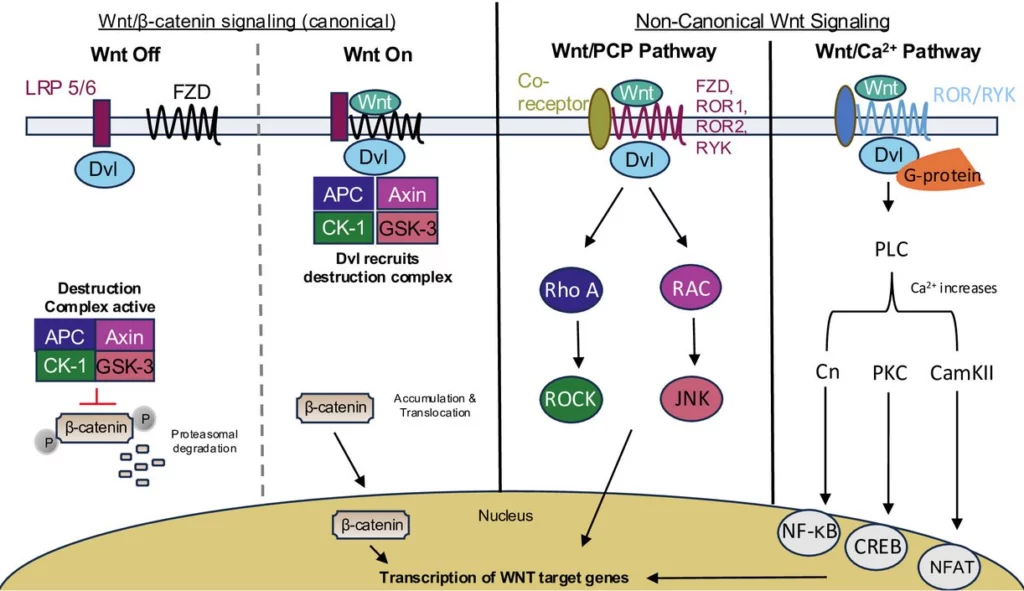
この経路は、細胞外リガンドであるWntタンパク質がFrizzled(FZD)受容体と共受容体LRP5/6に結合することで始まります。このシグナルによって、通常はβ-カテニンを分解する複合体(Axin、APC、GSK-3β、CK1α)が不活性化され、β-カテニンが細胞質内に安定化されます。
安定化したβ-カテニンは細胞核に移行し、LEF/TCFファミリーの転写因子と結合して、神経発達に関連するさまざまな遺伝子の発現を調節します。このプロセスには、以下のような転写調節因子も関与しています:
- 共活性化因子:CBP(CREBBP)、BCL9 など
- 転写抑制因子:Groucho、NCoR/SMRT複合体など
これらの因子の多くは、ASD患者で機能喪失型変異(loss-of-function)または機能亢進型変異(gain-of-function)が報告されており、遺伝子発現レベルでのシグナル調節異常が神経発達に及ぼす影響が示唆されています。
さらに、Wnt/β-カテニン経路は、Hedgehog、Notch、BMP、レチノイン酸経路など、他の発達経路と密接に連携しており、神経発達におけるシグナル伝達の複雑なネットワークを形成しています。
疾患名|Disorder
ASDは、神経発達に関わる状態のグループであり、以下のような特徴がみられます:
- 社会的な相互作用やコミュニケーションの持続的な困難
- 興味や行動がかたよる傾向、およびそれが繰り返されること
ASDは、その現れ方が非常に多様で、「スペクトラム(連続体)」という言葉が使われているように、症状の重さや範囲は人によって異なります。たとえば、早い時期からの大頭症(頭囲が平均より大きい状態)、言葉の発達の遅れ、感覚の過敏・鈍感、知的障がいをともなう場合など、多彩な特徴が組み合わさって現れることがあります。
最近の分子生物学的な研究では、Wnt/β-カテニン経路の異常が、ASDの中でも「症候性ASD(syndromic ASD)」と「特別な疾患に帰属しないASD(idiopathic ASD)」の両方に関連している可能性があると示唆されています。たとえば、CHD8、CTNNB1、TCF7L2といった遺伝子に見られる変異や、BCL9、CBPといった補助的な因子の調節異常が、ASDの根本的なメカニズムに深く関わっていると考えられています。
これらの遺伝的変化は、脳の発達スケジュールや神経前駆細胞の増殖、シナプスの成熟などに影響を与えることがわかってきており、こうした過程の乱れが、ASDの脳に見られる構造的・機能的な特徴につながっていると理解されています。
症状|Symptoms
Wnt/β-カテニン経路の調節異常によって引き起こされるASDの症状は、多くの場合、神経発達や行動に関わるさまざまな異常として現れます。以下のような特徴がみられることがありますが、人によって組み合わせや程度は異なります。これらの症状は、興奮性ニューロン、抑制性ニューロン、オリゴデンドロサイト前駆細胞など、脳のさまざまな細胞系列における機能不全を反映しており、これらはすべて、胎児期から生後早期の発達段階においてWntシグナルの影響を強く受ける細胞たちです。
大頭症(macrocephaly)
CHD8の機能喪失やβ-カテニンの安定化などにより、神経前駆細胞が過剰に増殖し、結果として頭囲が平均よりも大きくなることがあります。これはASDで比較的よく見られる身体的特徴の一つです。
繰り返しの行動や常同行動
動物モデルにおいて、WNT2の過剰発現によってドパミン系の神経が過剰に発達し、これに関連した反復的な行動が確認されています。
社会的相互作用の困難
抑制性ニューロンでβ-カテニンが欠損したマウスでは、他者とのやりとりが困難になるなど、社会性の障害が観察されています。また、ASDモデル動物であるBTBRマウスでは、DISC1という遺伝子の欠損とともに同様の傾向が報告されています。
認知機能の変化
物体認識や記憶の変化、大脳皮質の神経回路の変容などがみられることがあります。ヒトのASD脳組織や動物モデルでは、樹状突起スパインが過剰かつ未熟な状態で存在していることも観察されています。
大脳皮質の構造異常
ASDの患者さんでは、皮質のミニコラム(神経細胞の小さな縦の単位)の構造異常や、浅い層に神経細胞が過剰に存在し、深い層では密度が減少しているといった変化が報告されています。これらは、Wntシグナルの異常による早期の皮質形成異常と一致する所見です。
言語の発達の遅れ
まだ限られた研究ですが、患者さん由来のiPS細胞(人工多能性幹細胞)モデルから得られた知見では、Wnt/β-カテニン経路の活性が高まっているケースで、言語発達の遅れがみられる可能性があると報告されています。
疫学|Epidemiology
ASDは、世界人口のおよそ 1~2% に影響を及ぼすと報告されており、その頻度は国や地域、診断基準、調査方法などによってばらつきがあります。
ASDは、一般的に男性に多く診断される傾向があり、男女比はおよそ 4対1 とされています。ただし、これは女性における診断のされにくさが一因と考えられており、女性ではより目立ちにくい社会的・認知的な特徴を持つ傾向や、診断に結びつきにくい症状の表れ方が影響している可能性があります。実際、女性のASDでは、神経発達を調節する重要な遺伝子に「新生変異(de novo mutation)」が見られる頻度が高いという報告もあります。
Wnt/β-カテニン経路に関連する変異がASD全体の中でどのくらいの割合を占めるかは、現時点で明確に定まっていませんが、大規模なゲノム研究では、ASDに強く関連づけられている上位102個の遺伝子のうち、約59個 がWnt/β-カテニン経路と構造的または機能的に関係していることが示されています。そのうち少なくとも 18個の遺伝子 は、Wnt経路を抑制する役割を持つ「負の調節因子(negative regulators)」です。
また、人口別の解析からは、CHD8、CTNNB1、TCF7L2といったWnt経路の調節因子に新生変異が見られるASDの症例では、大頭症を伴うことが多いことや、重症型の表現型を持つ女性に多く見られる傾向があるとされています。
さらに、1歳から4歳の小児ASDコホート(集団)では、末梢血液中の白血球を用いた遺伝子発現解析において、Wnt/β-カテニン経路に関連する遺伝子の活性が高まっていることが明らかになりました。これは、Wnt経路の異常が中枢神経だけでなく、体全体に及んでいる可能性があることを示唆しており、将来的には非侵襲的な方法による早期診断のバイオマーカー開発につながるかもしれません。
ASDに関与する主要遺伝子|Key Genes Implicated in ASD via Wnt/β-Catenin Pathway
ASDに関連するとされる多くの遺伝子は、直接または間接的にWnt/β-カテニン経路の制御に関わっています。これらの遺伝子には、転写調節、シグナル受容、共抑制因子の制御、クロマチン再構成など、多様なレベルでの機能が含まれており、Wnt経路の恒常性を保つ上で重要な役割を果たしています。
以下に、主要な関連遺伝子とその機能的特徴をまとめます。
| 遺伝子名 | 染色体位置 | 機能 | 変異効果 | 備考 |
|---|---|---|---|---|
| CHD8 (Chromodomain Helicase DNA-binding Protein 8) |
14q11.2 | クロマチン構造の調整を通じて、Wntターゲット遺伝子の転写を抑制。 | 機能喪失型変異(LOF)により、β-カテニン依存性遺伝子の発現が過剰になり、神経前駆細胞の過剰増殖と大頭症(macrocephaly)を引き起こす。 | マウスにおいて同様の表現型が確認されている。 |
| CTNNB1 (Catenin Beta 1/β-カテニン遺伝子) |
3p22.1 | Wnt経路の中心シグナル分子であり、転写活性化に必須。 | 分解を妨げる変異により、β-カテニンが核に異常に蓄積し、皮質過成長・神経回路の異常形成を招く。 | GABA作動性介在ニューロンでのノックアウトは、社会的行動障害や記憶機能の変化と関連する。 |
| FZD9 (Frizzled Class Receptor 9) |
7q11.23 | Wntリガンド(特にWNT2)を受容するFrizzledファミリーの一員。 | コピー数変異(CNV)や点変異が、ドパミン作動性ニューロンの発達異常と常同行動の増加に関係しているとされる。 | — |
| WNT2 (Wnt Family Member 2) |
7q31 | Wntファミリーの一員で、ASDのコホート研究で高頻度の変異が検出されている。 | 過剰発現により、ドパミン系の過形成や反復行動の増加と関連。 | — |
| TCF7L2 (Transcription Factor 7 Like 2) |
10q25.2-q25.3 | β-カテニンと共に働くLEF/TCFファミリーの転写因子。皮質形成、オリゴデンドロサイト分化、視床皮質接続に重要。 | ASDに関連する新生変異(de novo variants)が複数報告されている。 | — |
| BCL9 および CBP (CREBBP) |
1q21.2および16p13.3 | β-カテニンと結合して転写活性を促進する共活性化因子。 | ASD患者において欠失または重複変異が観察されている。 | — |
| UBE3A (Ubiquitin Protein Ligase E3A) |
15q11–q13 (Angelman症候群関連領域) |
— | p.T485A変異により、Wnt経路が活性化される。ASD様の症状を伴う表現型が見られることがある。 | — |
| TBL1XR1 (Transducin Beta Like 1 X-Linked Receptor 1) |
3q26.32 | 共抑制複合体(nuclear co-repressor)を介して、β-カテニンの転写活性を調節。 | Wntの過剰活性化およびASD様表現型との関連が示されている。 | — |
| MED13L (Mediator Complex Subunit 13 Like) |
12q24.21 | メディエーター複合体を介して転写制御に関与。TBL1XR1と共に、遺伝子発現の精密な調整に寄与。 | ASDおよび類縁疾患に関わる異常が報告されている。 | — |
ASDの病因:遺伝的および環境的要因の統合|Etiology of ASD: Genetic and Environmental Integration
自閉スペクトラム症(ASD)は、単一の原因ではなく、複数の遺伝的要因と環境因子が相互に作用することで発症する多因子性の神経発達障害です。特に、ASDにおいて中心的役割を果たすとされるカノニカルWnt/β-カテニン経路は、その両方の影響を受けやすい分子経路のひとつとして注目されています。
遺伝的メカニズム
Wnt/β-カテニン経路の調節に関わる遺伝子群において、以下のようなメカニズムでASDの病因が説明されています:
CHD8の機能喪失型変異(LOF)
クロマチン再構成因子CHD8は、β-カテニン依存性遺伝子の転写を抑制します。変異によりこの機能が低下すると、Wnt経路が過剰に活性化し、神経前駆細胞の増殖異常と大頭症を引き起こします。これはASDで観察される脳過成長と一致します。
CTNNB1の変異
β-カテニンをコードするCTNNB1に変異が起こると、β-カテニンの分解が妨げられ、異常な核内蓄積と転写活性が生じます。これは皮質過成長や神経回路の過形成を導き、社会性の障害や記憶機能の変化にも関与します。
FZD9のCNVとWNT2の過剰発現
これらの変異は、ドパミン作動性神経回路の異常を引き起こし、繰り返し行動(repetitive behaviors)の増加など、ASDに特有の行動表現型と関係します。
TCF7L2やBCL9など転写因子の異常
Wnt経路の下流で遺伝子発現を調節する転写因子の変異は、皮質形成やオリゴデンドロサイト分化、視床皮質接続において機能障害を生じさせる可能性があります。
UBE3A(p.T485A変異)およびTBL1XR1の変異
これらは異なるメカニズムでWnt経路を過剰に活性化することが知られており、ASDに加えてAngelman症候群などの関連神経発達症でも同様の症状が報告されています。
環境要因とWnt経路の撹乱
ASDの発症リスクを高める環境因子の中には、発達中のWnt/β-カテニン経路に直接的な影響を与えることが動物実験等で示されています。
バルプロ酸(Valproic Acid:VPA)
妊娠中のVPA曝露は、動物モデルにおいてWNT1およびWNT2の発現上昇を引き起こし、ASD様行動と神経発達異常を誘導します。ヒトでもVPA曝露とASD発症リスクとの相関が報告されています。
選択的セロトニン再取り込み阻害薬(SSRIs)
一部の抗うつ薬(SSRIs)はWnt経路を活性化することが示唆されており、妊娠中の使用がASD発症リスクと関係する可能性があるとする研究も存在します。ただし、これらの知見には集団差や交絡因子があるため、慎重な解釈が求められます。
総括
Wnt/β-カテニン経路は、ASDの病態において遺伝子と環境の交差点として機能しており、この経路の調節異常は、神経前駆細胞の過剰増殖や神経接続の異常、行動表現型の多様性に大きく寄与することが示されています。
このような知見は、ASDの理解を「単なる行動症候群」から「シグナル経路中心の発達異常症候群」へと再定義する手がかりとなり、個別化医療(precision medicine)やバイオマーカーの開発への応用が期待されます。
検査・診断|Testing & Diagnosis
自閉スペクトラム症(ASD)の診断は、現在のところ臨床的評価が中心で行われており、行動観察や発達歴に基づく詳細な評価が用いられます。標準的な診断ツールには、以下のようなものがあります:
- ADOS(Autism Diagnostic Observation Schedule):ASDの特性を直接観察するための標準化された行動評価
- ADI-R(Autism Diagnostic Interview-Revised):保護者へのインタビューを通じて、社会性や行動の特徴を評価
これらの方法によって、社会的コミュニケーションの困難さや、興味・行動の限定性・反復性など、ASDの中核的な特徴を多角的に確認していきます。
一方で、近年の研究では、Wnt/β-カテニン経路の異常がASDに深く関わっていることが示されており、将来的にはこうした分子レベルの指標(バイオマーカー)が、従来の行動評価を補完する可能性があると期待されています。ここでは、現在注目されている検査手法をご紹介します:
末梢血のバイオマーカー
1~4歳のASD児における白血球(末梢血)の遺伝子発現を調べたところ、Wnt/β-カテニン経路に関わる遺伝子の活性化が確認されました。これは、神経組織ではない体の細胞でもシグナル異常が反映されている可能性を示しており、非侵襲的かつ早期に検出可能な診断法の開発につながるかもしれません。
遺伝子検査
ASDに強く関与しているとされるWnt経路関連遺伝子(例:CHD8、CTNNB1、TCF7L2、BCL9など)は、次世代シーケンシング(NGS)を用いた遺伝子パネル検査や、全エクソーム/全ゲノム解析の対象として取り上げられつつあります。特に、大頭症を伴うASDや、その他の症候を含む「症候性ASD」においては、遺伝子診断が有効な手がかりとなる場合があります。
iPS細胞を用いた細胞モデル
患者さん由来のiPS細胞(人工多能性幹細胞)を神経前駆細胞やニューロンに分化させて、Wnt経路の機能を直接評価する試みも進められています。これにより、個別の患者さんごとの疾患の進行や重症度の理解が深まる可能性があります。
現時点では、ASDの診断に用いるWnt活性の臨床認可済みバイオマーカーは存在していませんが、Wnt経路の代表的な転写標的であるAxin2などが、診断マーカー候補として研究されています。また、神経幹細胞や皮質組織における遺伝子発現パターンも、将来的に診断や予後予測に役立つ可能性が期待されています。
治療法と管理|Treatment & Management
現在のところ、Wnt/β-カテニン経路を直接的に標的とするASD治療薬は、米国食品医薬品局(FDA)によって承認されていません。しかし、動物モデルや前臨床研究では、この経路の活動を調整することによりASDの症状を部分的に改善できる可能性が示唆されています。
以下は、研究段階で検討されている治療戦略の概要です。
経路抑制薬(Pathway Inhibitors)
Wnt/β-カテニン経路が過剰に活性化しているタイプのASDでは、その活動を抑えることで症状が改善される可能性があります。
- Tankyrase阻害薬(例:XAV939)
β-カテニンの分解を促進する「破壊複合体」を安定化させ、Wntシグナルを抑制します。動物モデルでは、この薬剤を使ってASD様行動を再現する実験も行われています。 - Porcupine阻害薬(例:LGK974/WNT974)
Wntリガンドの分泌を妨げることで、経路全体の活性を抑えます。現在はがん治療薬として臨床試験中ですが、将来的にASDへの応用も検討される可能性があります。 - Β-カテニンと共活性化因子の結合阻害薬
CBP/p300、BCL9、TCFなどとの結合を妨げ、異常な遺伝子発現を抑制するアプローチです。
経路活性化薬(Pathway Activators)
Wntシグナルが過少である場合、この経路を適切に活性化することで、神経幹細胞の機能やシナプス形成を回復できる可能性があります。
- リチウム
GSK-3βを阻害することで、β-カテニンの安定性を高めます。もともとは双極性障害の治療薬ですが、神経細胞へのWntシグナル活性にも影響します。 - バルプロ酸(VPA)
WNT1やWNT2の発現を高める作用があり、妊娠中の曝露はASDリスクと関連しますが、別の文脈ではヒストン脱アセチル化酵素(HDAC)阻害作用により神経新生を促す可能性もあります。 - CHIR99021
GSK-3βを選択的に阻害する薬剤で、ドパミン神経の発達を促すことが動物実験で示されています。 - SSRI(選択的セロトニン再取り込み阻害薬)
Wnt経路を活性化する作用が試験管内で確認されています。ただし、妊娠中の使用とASDリスクの関連性が一部の集団で報告されており、慎重な検討が必要です。
その他の調節因子
- イマチニブ(Imatinib):チロシンキナーゼ阻害薬であり、Wnt/β-カテニン経路を抑制することで、行動や神経機能の改善が期待されています。
- レチノイン酸(RA)やHedgehog経路の調節薬:Wnt経路と相互作用を持ち、併用療法の候補として研究が進められています。
臨床における留意点
現時点では、ASDを対象としたWnt経路標的治療薬の臨床試験は実施されていません。Wnt経路は、発達中の臓器や組織の恒常性にも関与しているため、治療の適用には時期や標的組織を限定した精密な設計が求められます。こうした背景から、個別化医療(personalized medicine)の重要性が高まっており、Wnt経路の活性状態や関連遺伝子の発現を評価した上で薬剤を選択するアプローチが、今後必要になると考えられます。
予後|Prognosis
自閉スペクトラム症(ASD)の予後(将来の見通し)は、症状の重さ、発達の段階での早期介入の有無、そして併存する医学的・発達的な状態など、さまざまな要因によって大きく異なります。
今回ご紹介している文献では、Wnt/β-カテニン経路の変異に直接結びついた長期的な予後データはまだ十分に蓄積されていませんが、いくつかの重要な知見が報告されています。
まず、CHD8変異などによってWnt活性が高まっている場合、大頭症の出現やより早期のASD症状の発現、さらに「症候性ASD(syndromic ASD)」としての診断に至るケースが多いことが示されています。これらのケースでは、より複雑な臨床経過をたどる可能性があるため、継続的かつ個別化された支援が重要です。
また、Wnt関連遺伝子の変異を持つ方々では、症状のあらわれ方に幅があり、それに応じて治療への反応にも違いが生じる可能性があります。たとえば、特定の経路分子に作用する薬剤が、有効性を示すケースとそうでないケースが存在し、分子レベルでの個別診断や治療の最適化が、今後ますます重要になると考えられています。
動物モデルを用いた研究では、Wnt経路を調整する薬剤(例:GSK-3β阻害薬)を発達の早い時期に投与することで、ASDに類似した行動や神経学的異常が一部回復することが示唆されています。これは、適切な時期に介入することによって、発達の流れを変える可能性があることを示しており、早期診断と支援の重要性を裏づける結果といえます。
さらに、Wnt経路の活性状態を反映するバイオマーカー(例:Axin2の発現や、白血球における遺伝子発現プロファイルなど)が将来的に個別の予後予測に役立つ可能性も示されています。これにより、より精密な支援計画の立案が可能になることが期待されます。
全体として、Wnt/β-カテニン経路の調節異常は、ASDの背景にある一貫した、かつ生物学的にもっともらしい要因として注目されていますが、それが個々の長期的な経過にどのように影響するかについては、今も研究が進められている段階です。
現在得られている知見は、ASDの早期発見と介入の重要性、そしてそれぞれの方の遺伝的・分子的特徴に合わせたきめ細やかな支援の必要性を示しており、私たちが今後のケアをより良いものにしていくための大切な道しるべとなります。
引用文献|References
- Baranova, J., Dragunas, G., Botellho, M.C.S. et al. Autism Spectrum Disorder: Signaling Pathways and Prospective Therapeutic Targets. Cell Mol Neurobiol 41, 619–649 (2021). https://doi.org/10.1007/s10571-020-00882-7
- Nadin, Silvina B., et al. ‘Overview of Wnt/β-Catenin Pathway and DNA Damage/Repair in Cancer’. Biology, vol. 14, no. 2, Feb. 2025, p. 185. DOI.org (Crossref), https://doi.org/10.3390/biology14020185.
- Clevers, Hans, and Roel Nusse. ‘Wnt/β-Catenin Signaling and Disease’. Cell, vol. 149, no. 6, Jun. 2012, pp. 1192–205. DOI.org (Crossref), https://doi.org/10.1016/j.cell.2012.05.012.
- MacDonald, B. T., Tamai, K., & He, X. (2009). Wnt/beta-catenin signaling: components, mechanisms, and diseases. Developmental cell, 17(1), 9–26. https://doi.org/10.1016/j.devcel.2009.06.016
- Gao, Juanmei, et al. ‘Wnt/β-Catenin Signaling in Neural Stem Cell Homeostasis and Neurological Diseases’. The Neuroscientist, vol. 27, no. 1, Feb. 2021, pp. 58–72. DOI.org (Crossref), https://doi.org/10.1177/1073858420914509.
- Pascual, Danielle M., et al. ‘Excess Wnt in Neurological Disease’. Biochemical Journal, vol. 482, no. 10, May 2025, pp. 601–18. DOI.org (Crossref), https://doi.org/10.1042/BCJ20240265.
- Caracci, Mario O., et al. ‘Wnt/β-Catenin-Dependent Transcription in Autism Spectrum Disorders’. Frontiers in Molecular Neuroscience, vol. 14, Nov. 2021, p. 764756. DOI.org (Crossref), https://doi.org/10.3389/fnmol.2021.764756.
- Upadhyay, Jyoti, et al. ‘Dysregulation of Multiple Signaling Neurodevelopmental Pathways during Embryogenesis: A Possible Cause of Autism Spectrum Disorder’. Cells, vol. 10, no. 4, Apr. 2021, p. 958. DOI.org (Crossref), https://doi.org/10.3390/cells10040958.
- Liu, J., Xiao, Q., Xiao, J. et al. Wnt/β-catenin signalling: function, biological mechanisms, and therapeutic opportunities. Sig Transduct Target Ther 7, 3 (2022). https://doi.org/10.1038/s41392-021-00762-6