神经传递的微小变化为何会影响发育的方式
简明总结
自闭症谱系障碍(ASD)是一种神经发育障碍,在语言、眼神交流、感官接受方式等方面表现出一些大脑功能上的特征。本文将以浅显易懂的方式介绍一种被认为与ASD背景相关的大脑物质——GABA(γ-氨基丁酸)。
GABA具有使大脑神经的兴奋平静下来、促进信息顺畅传递的作用。在儿童大脑发育的过程中,GABA有时会暂时起到相反的作用,帮助兴奋。如果这种转换未能顺利进行,就可能更容易出现类似ASD的特征。遗传因素(如SLC12A5、MECP2等)以及大脑内的离子平衡也有着密切关系。
本文尽可能通俗地介绍了与ASD相关的机制、常见症状、检查和诊断的方法、治疗和支持的可能性,以及未来的展望。希望能为孩子和家庭的理解与支持提供一些帮助。
概要|Overview
GABA(γ-氨基丁酸,γ-aminobutyric acid)是成熟哺乳动物大脑中主要的“抑制性神经递质”。它具有让神经细胞活动安静下来的作用,对于大脑回路的正确形成及信息的正常传递至关重要。
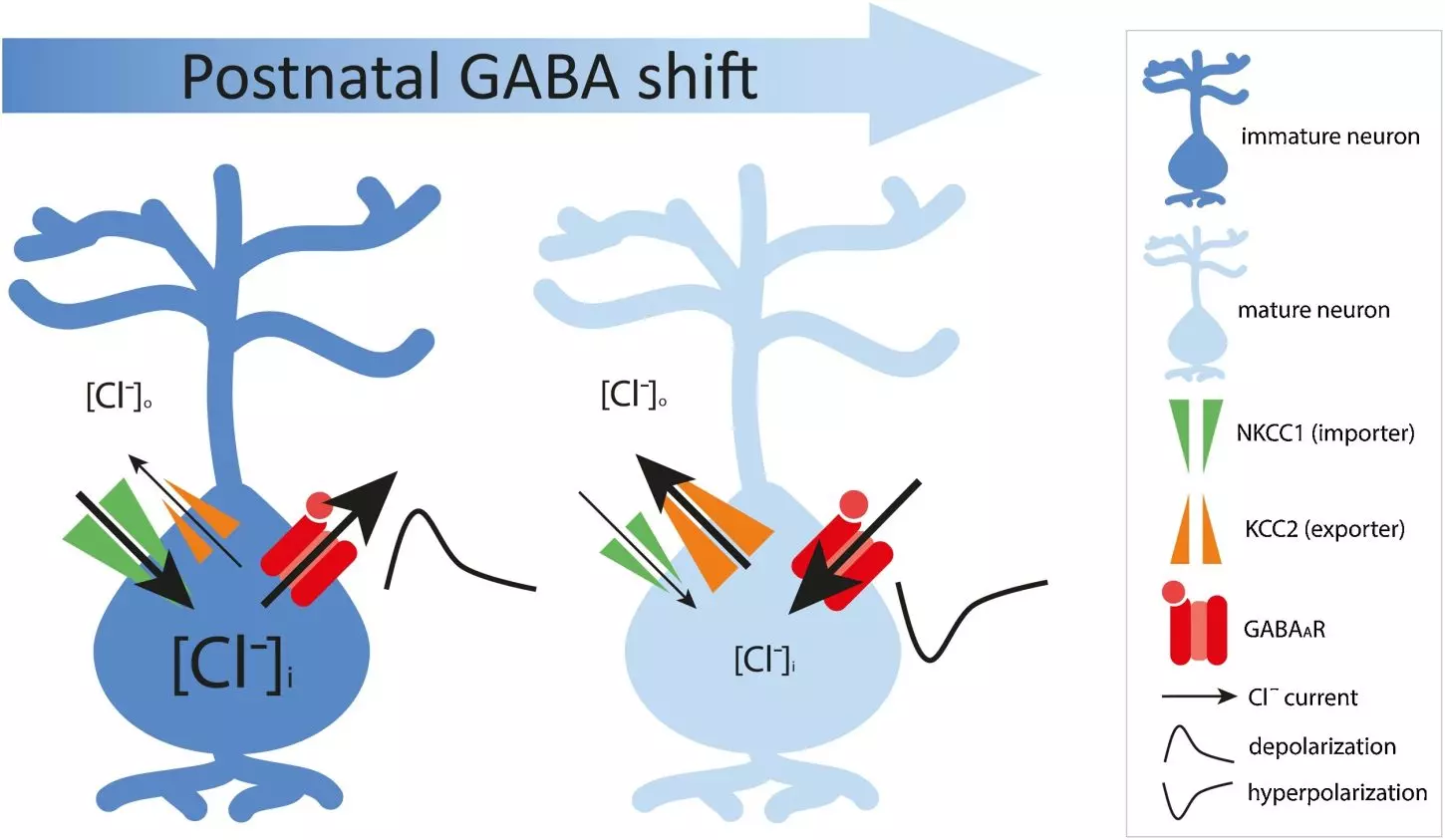
在出生后不久的大脑中,GABA信号暂时表现为“兴奋性(去极化,depolarizing)”。这是因为神经细胞内存在大量的氯离子(Cl⁻),并且由NKCC1这种氯离子输入转运蛋白维持这种状态。
随着大脑发育,KCC2这种将氯离子排出细胞外的转运蛋白逐渐增加,GABA的作用会转变为“抑制性(超极化,hyperpolarizing)”。这种转换被称为“出生后的GABA极性转换(postnatal GABA shift)”,是神经回路发育中极为关键的过程。
这种GABA的转换不仅仅是化学变化,还深刻参与了神经细胞的增殖、分化、迁移、突触的形成与修剪,以及整个神经网络的节律(网络振荡)和兴奋—抑制平衡(excitation/inhibition balance,E/I平衡)。
当这种转换的时机、位置或程度不正常时,研究表明会与自闭谱系障碍(Autism Spectrum Disorder,ASD)等多种神经发育障碍(Neurodevelopmental Disorders,NDDs)相关。
实际上,在ASD的动物模型和患者研究中发现,GABA的功能不足以及过度活跃的情况都有出现。这些异常与GABA受体(GABA receptors)、氯离子转运体以及信号调节因子的基因突变有关。
更重要的是,这些与GABA相关的异常与调控神经细胞生长、代谢、可塑性(适应性变化能力)的“PI3K–AKT–mTOR通路”有紧密交互。这一路径的异常同样被认为是ASD等疾病发病机制中的重要因素。
遗传基因区域|Implicated Genomic Region
GABA功能异常被发现与多种基因区域的异常有关。这些基因编码GABA受体的组成部分、调节氯离子进出的转运蛋白、突触相关蛋白及转录因子等。
例如,15q11–q13区域常在ASD中出现“重复(duplication)”。该区域包含编码GABA<sub>A</sub>受体亚基的基因,如GABRB3、GABRA5和GABRG3。此外,该区域还有调节突触形成的UBE3A基因,相关疾病被称为“Dup15q综合征(Dup15q syndrome)”。
决定GABA极性(从兴奋性转换为抑制性)的主要氯离子共转运蛋白KCC2(SLC12A5)和NKCC1(SLC12A2)也至关重要。这些基因的突变或表达异常,会导致GABA应转为抑制性时依然保持兴奋性,从而引起神经回路的过度兴奋或异常发育。
另一个与GABA通路互相作用的重要分子通路是PI3K–AKT–mTOR通路。PTEN、TSC1、TSC2、NF1等基因参与该通路,调控神经的兴奋性、蛋白质合成及氯离子转运体的表达。
此外,已知与ASD相关的MECP2、FMR1、SHANK1/2/3、CNTNAP2/3/4、CDKL5等基因,也与GABA能突触的形成、抑制性中间神经元(interneuron)的功能及E/I平衡的维持密切相关。
其他如GABA合成相关的GAD1/2(编码谷氨酸脱羧酶)、稳定突触结构的GPHN(gephyrin)、突触黏附分子NRXN1–3(neurexin)及neuroligin 2也深度参与GABA受体的定位和稳定性。
这些遗传因素通常不会单独决定疾病的发生,多数情况下会与表观遗传因素、环境因素及性别差异共同作用。尤其值得关注的是,通过BDNF(脑源性神经营养因子)及其受体TrkB调控KCC2的机制,这一机制在实验模型和临床研究中均被反复证实。
疾病名称|Disorder
GABA功能异常涉及的代表性疾病是“自闭谱系障碍(Autism Spectrum Disorder,ASD)”。ASD是一种高度多样性的神经发育障碍,症状和困扰在不同个体间差异巨大。
该疾病的特征包括在语言、表情、肢体动作等“社会互动”方面的困难,以及对某些兴趣的强烈执着或重复性行为。
许多ASD个体还会伴随癫痫、智力发育迟缓(智力障碍)、注意缺陷多动障碍(ADHD)、睡眠障碍或感官过敏等“共病症状(comorbidities)”。这些症状均与大脑“兴奋—抑制平衡(E/I平衡)”的失调相关。
GABA功能异常直接影响这种平衡,它既可能是原因,也可能是结果。也就是说,早期GABA异常会影响大脑发育并表现为ASD特征;或者其他基因或环境因素改变了大脑,从而二次性地导致GABA失衡。
一些由特定基因突变或染色体异常引起的“综合征性ASD(syndromic autism)”几乎都伴有GABA通路的异常,例如:
- Rett综合征(Rett syndrome):由MECP2基因突变导致,主要影响女性。
- 脆性X综合征(Fragile X syndrome):由FMR1基因功能降低引起,伴有智力障碍的ASD类型。
- Angelman综合征(Angelman syndrome):由UBE3A基因异常引起,伴有严重发育障碍。
- CDKL5缺陷综合征(CDKL5 deficiency disorder):罕见疾病,伴有癫痫及严重神经发育迟滞。
- Dup15q综合征(Duplication 15q syndrome):由GABA受体相关基因重复引发,表现出ASD样特征。
- 唐氏综合征(Down syndrome):由于21号染色体重复,报道显示NKCC1表达异常。
- Dravet综合征(Dravet syndrome):由SCN1A基因突变引起,影响GABA抑制性神经元功能的癫痫综合征。
这些综合征有共同特点:GABA为核心的神经回路功能障碍、氯离子稳态紊乱(chloride homeostasis disruption)、以及大脑过度兴奋(network hyperexcitability)。这些症状往往还与PI3K–AKT–mTOR通路等发育信号通路异常相关。
流行病学|Epidemiology
自闭谱系障碍(ASD)是全球最常见的神经发育障碍之一,统计显示约每36名儿童中就有1人被诊断为ASD。
ASD存在明显的性别差异,男性的诊断率约为女性的3至4倍。原因尚未完全阐明,但研究推测GABA功能或氯离子转运体的表达时间差异可能是因素之一。例如有研究报告指出,女童的GABA“抑制性”转换发生得更早。
约20–30%的ASD个体伴有癫痫。这可能反映了大脑“兴奋—抑制平衡(E/I平衡)”调节不当。
此外,智力障碍、ADHD、睡眠障碍、感官过敏等与GABA功能异常相关的症状也常见于ASD个体。
虽然大部分ASD病例是多基因和环境交互作用的结果,但少数“综合征性ASD”有明确的单基因或染色体异常。这类病例的分子机制往往指向GABA通路功能障碍或氯离子稳态失调,成为研究ASD分子病理的重要线索。
病因|Etiology
ASD及其他神经发育障碍(NDDs)的成因复杂多样,既涉及基因变异,也包括环境因素及神经回路和细胞功能的多层次异常。
研究发现,GABA功能异常及氯离子稳态失衡是多数病例的共同机制,可从两方面理解:
1. 氯离子转运体失衡与GABA极性转换失败
胎儿期至新生儿早期,大脑中的GABA本应呈现“兴奋性(去极化)”,促进神经细胞的生长与迁移。此时神经细胞内Cl⁻含量高,由NKCC1(SLC12A2)介导。
发育后期,KCC2(SLC12A5)的功能增强,细胞内Cl⁻浓度下降,GABA转换为“抑制性(超极化)”。这一时机的切换对神经回路的成熟、感官处理及行为调节至关重要。
如果这一“GABA极性转换(GABA polarity shift)”延迟或失败,GABA无法抑制神经活动,反而促进过度兴奋,导致ASD特征或感官过敏。反之,如果抑制化发生得过早(KCC2过度表达或NKCC1过早消失),神经迁移及回路可塑性会受损。这类异常在Rett综合征、脆性X综合征、CDKL5缺陷综合征及环境因素(如孕期炎症或丙戊酸暴露)模型中均有观察。
2. GABA通路与mTOR通路的遗传及分子异常
多数ASD风险基因影响GABA功能或调控,包括:
- GABA受体亚基:GABRB3、GABRA5、GABRG3
- GABA合成与运输:GAD1/2、VGAT、gephyrin
- 氯离子转运体:KCC2、NKCC1
- 突触黏附分子:NRXN1–3、neuroligin(如NLGN2)
- 转录调控因子:MECP2、TCF4、CHD8
PI3K–AKT–mTOR通路同样高度相关:
- PTEN、TSC1/2、NF1等是mTOR抑制因子,突变会导致蛋白质合成过度,突触调控失衡。
- SHANK3、UBE3A、CHD8影响GABA突触结构数量并可激活mTOR通路。
- MECP2(Rett综合征基因)通过BDNF–TrkB通路调控KCC2表达,影响GABA极性转换。
环境因素如丙戊酸暴露、孕期炎症、氧化应激也可通过改变氯离子转运或激活脑内小胶质细胞,影响GABA的发育。
症状|Symptoms
如果GABA的功能在脑部发育的关键时期出现紊乱,便可能导致自闭症谱系障碍(ASD)以及其他神经发育障碍中常见的多种症状。这些症状不仅仅反映单个神经细胞的问题,还反映整个大脑网络的功能、节律(脑电活动)以及可塑性(适应变化的能力)的异常。
主要行为特征
1. 社会交往困难
前额叶、颞叶等脑区的E/I平衡失调被认为是重要原因。尤其是当PV+抑制性中间神经元功能减弱时,大脑处理社会信息所需的神经同步性会受损。
2. 对特定兴趣的执着及重复行为
GABA-A受体或其转运蛋白异常的小鼠模型中也观察到了类似的重复行为。
3. 感官过敏(尤其是触觉和听觉)
如果GABA在丘脑—皮质回路中的调节功能受损,个体便难以调节外界刺激的强度,从而表现出感官过敏。
神经学共病
1. 癫痫与抽搐发作
如果GABA长期保持兴奋性状态,细胞无法有效排出Cl⁻,便会导致神经过度兴奋,从而引发癫痫发作(如Dravet综合征、Rett综合征)。
2. 智力障碍
GABA功能异常会阻碍神经回路的精细化(突触修剪)与网络形成,导致学习、记忆等功能发育不足。
3. 睡眠障碍
当GABA在下丘脑或脑干的功能被扰乱时,生物钟及睡眠节律可能受到影响。
神经生理特征
1. 伽马波(30–80Hz)减少
PV+抑制性中间神经元活动下降会导致高频脑波(伽马波)降低,使信息处理效率下降。
2. GABA极性转换延迟或异常
神经网络失去同步性,“巨大去极化电位(GDPs)”等异常活动持续存在。
3. 脑电(EEG)模式异常
ASD个体的EEG频谱往往波动更大,伽马频段一致性降低。
性别及脑区差异
- 女童的GABA极性转换更早
这被认为部分解释了ASD的性别差异。 - 脑区特异性
不同脑区的GABA相关标记物及氯离子转运蛋白异常表现不同,如前扣带皮质、海马体、视觉皮质等。
综合来看,GABA功能异常相关症状往往由发育时序的错位及脑区脆弱性的叠加所致。抑制不足(disinhibition)是这些多样症状的核心机制。
检查与诊断|Testing & Diagnosis
目前,自闭症谱系障碍(ASD)的诊断主要基于临床观察与行为评估。国际上通常依据《DSM-5(精神障碍诊断与统计手册第5版)》的标准,确认社会交往障碍及有限、重复性行为或兴趣的存在。
随着研究进展,科学家尝试通过生物标志物进行分层(stratification),为未来的精准医学(precision medicine)打下基础。
脑影像与神经生理标志物
磁共振波谱(Magnetic Resonance Spectroscopy, MRS)
这是一种无创检测技术,可量化特定脑区的GABA浓度。ASD研究显示,在前扣带皮质、前额叶皮质及体感皮质区域,GABA/谷氨酸比值(GABA/glutamate ratio)有下降趋势,但结果随年龄和个体差异而异。
脑电图(Electroencephalography, EEG)
EEG研究发现,ASD个体常表现出伽马波幅度降低、频谱斜率异常及E/I平衡波动增加等模式。这些指标未来可能成为分型或疗效预测的工具。
双眼视野竞争实验(Binocular Rivalry Paradigm)
ASD个体的视觉处理速度与GABA浓度之间的相关性减弱,提示视觉皮质的抑制功能失衡。
解剖学与遗传学发现
尸检脑组织研究发现:
- PV+抑制性中间神经元数量减少
- GABA合成酶GAD65/67下降
- KCC2或GABA受体基因的表观遗传下调
这些都指向抑制性神经传递的降低。
虽然基因检测不是ASD诊断的常规步骤,但部分病例可发现:
- 单基因突变:MECP2、FMR1、SHANK3
- GABA相关基因的单核苷酸多态性(SNPs):如GABRB3、GABRA5、SLC12A5
- 染色体结构变化(拷贝数变异,CNVs):如Dup15q综合征
这些信息有助于诊断综合征性ASD,并指导个体化治疗。
治疗与管理|Treatment & Management
目前针对自闭症谱系障碍(ASD)的药物有限,主要集中在处理伴随症状,如易激惹、癫痫或睡眠障碍。
然而,近年来针对GABA功能异常及氯离子稳态失衡的治疗探索快速发展,从动物实验到临床试验均有涉及。
1. 针对氯离子转运体的治疗
布美他尼(Bumetanide)
布美他尼是一种选择性抑制NKCC1(钠-钾-氯共转运体1)的利尿剂,可降低神经细胞内Cl⁻浓度,从而帮助GABA从“兴奋性”向“抑制性”转换。
- 动物模型:改善行为与神经网络异常。
- 临床研究:小规模试验表明部分儿童症状有改善,尤其是伴随EEG异常或炎症指标升高的个体。
- 局限性:血脑屏障通透性弱,副作用包括低钾血症、脱水,需严格监测。
KCC2激活剂
尚处于前临床阶段,如CLP257等药物有望增强Cl⁻外排,恢复GABA的抑制作用,并改善突触可塑性。
2. 调节GABA受体的药物
GABA-A受体激动剂或调节剂
如Gaboxadol或苯二氮䓬类药物,可增强GABA的持续性抑制(tonic inhibition),但疗效个体差异大,有的患者会出现嗜睡,有的则焦虑加剧。
GABA-B受体激动剂(如巴克洛芬,Baclofen)
动物模型显示可减少重复行为并改善脑电活动,临床前景被看好。
3. 针对分子通路的治疗
PI3K–AKT–mTOR通路调控
在结节性硬化症或PTEN突变相关的ASD病例中,雷帕霉素衍生物(如依维莫司)可改善E/I平衡及网络同步性。
BDNF–TrkB通路调控
通过刺激此通路,可促进KCC2表达,帮助GABA极性转换。
4. 基因与细胞治疗
基因治疗
在Rett综合征模型中,重新激活MECP2基因可部分恢复GABA传递及行为功能。
细胞治疗
将胚胎内侧神经节区(MGE)来源的中间神经元移植至模型动物脑中,能够恢复抑制功能与社交行为。
5. 非药物干预
感官刺激丰富化(sensory enrichment)
动物实验表明,通过增加环境刺激,可促进KCC2表达并恢复抑制性神经功能。
其他方法
饮食控制、运动训练,以及经颅直流刺激(tDCS)或经颅磁刺激(TMS)等神经调控方法,也在研究探索阶段。
预后|Prognosis
自闭症谱系障碍(ASD)的预后差异很大,与GABA功能及神经回路异常的发生时间和程度密切相关。
有利因素
- GABA极性转换发生时得到早期支持
- 无明显智力障碍或语言障碍
- 明确的基因背景,如KCC2/NKCC1失衡,可针对性应用布美他尼等药物
持续困难的风险因素
- GABA极性转换显著延迟或缺失,导致神经回路结构永久错配
- 伴癫痫的ASD(如Rett、Dravet)往往症状更重
- 青春期后的激素变化、环境压力或慢性炎症可能进一步影响GABA系统
神经可塑性与补偿力
尽管存在早期功能障碍,大脑具备恢复和补偿能力。通过经验学习,患者可建立替代性神经通路并适应社会生活。适当的支持和环境干预可显著增强这种可塑性。
结论|Conclusion
深入理解GABA这一神经递质的机制,是揭开ASD等复杂神经发育障碍机制的关键。GABA受体、氯离子转运体及PI3K–AKT–mTOR通路相互协作,维持微妙的兴奋与抑制平衡。然而,这种平衡极易被时间微差、基因变异或炎症反应打破。
研究表明,这并非“注定的命运”,而是脆弱与恢复力的角力。即便GABA未能顺利转为抑制性,或中间神经元迁移出现障碍,大脑也会尝试寻找新的路径以实现适应。
重要的是,功能表面正常并不意味着个体不需要支持。支持需求不应仅仅通过症状表象来衡量,每一段发展经历都值得关注与理解。
人类神经系统复杂而脆弱,却又惊人地灵活。在这种微妙的平衡中,人类能够感知、学习、爱与赋予意义。哪怕平衡有偏差,这也不意味着失去了发展的可能。
参考文献|References
- Topchiy, Irina, et al. “GABA System as the Cause and Effect in Early Development”. Neuroscience & Biobehavioral Reviews, vol. 161, Jun. 2024, p. 105651. https://doi.org/10.1016/j.neubiorev.2024.105651.
- Bruni, Oliviero, et al. “Herbal Remedies and Their Possible Effect on the GABAergic System and Sleep”. Nutrients, vol. 13, no. 2, Feb. 2021, p. 530. https://doi.org/10.3390/nu13020530.
- Tang, X., Jaenisch, R. & Sur, M. “The role of GABAergic signalling in neurodevelopmental disorders”. Nat Rev Neurosci 22, 290–307 (2021). https://doi.org/10.1038/s41583-021-00443-x.
- Zhao, Haisheng, et al. “GABAergic System Dysfunction in Autism Spectrum Disorders”. Frontiers in Cell and Developmental Biology, vol. 9, Feb. 2022, p. 781327. https://doi.org/10.3389/fcell.2021.781327.
- Cherubini, Enrico, et al. “Dysregulation of GABAergic Signaling in Neurodevelopmental Disorders: Targeting Cation-Chloride Co-Transporters to Re-Establish a Proper E/I Balance”. Frontiers in Cellular Neuroscience, vol. 15, Jan. 2022, p. 813441. https://doi.org/10.3389/fncel.2021.813441.
- Ferranti, Anthony S., et al. “Novel Pharmacological Targets for GABAergic Dysfunction in ADHD”. Neuropharmacology, vol. 249, May 2024, p. 109897. https://doi.org/10.1016/j.neuropharm.2024.109897.
- Giniatullin, Rashid, and Enrico Cherubini. “Gabaergic Signalling in Autism Spectrum Disorders (ASD): Role of Glial Cells and Therapeutic Perspectives”. Brain, Behavior, and Immunity, vol. 129, Oct. 2025, pp. 681–89. https://doi.org/10.1016/j.bbi.2025.07.003.
- Peerboom, Carlijn, and Corette J. Wierenga. “The Postnatal GABA Shift: A Developmental Perspective”. Neuroscience & Biobehavioral Reviews, vol. 124, May 2021, pp. 179–92. https://doi.org/10.1016/j.neubiorev.2021.01.024.
术语解释|Helpful Terms
NKCC1(SLC12A2)
将Cl⁻运入神经细胞的转运体,胎儿及新生儿期大量表达,使GABA在该阶段呈兴奋性。
自闭谱系障碍(Autism Spectrum Disorder, ASD)
一种神经发育模式不同的状态,社会交往、感官处理、兴趣或行为模式有显著差异。症状表现和程度差异极大,智力水平及语言能力范围广泛。
神经发育障碍(Neurodevelopmental Disorder)
涉及脑发育过程异常的一类疾病,包括ASD、注意缺陷多动障碍(ADHD)、智力发育障碍等,由遗传、环境及其他多种因素共同作用。
GABA(γ-氨基丁酸,Gamma-Amino Butyric Acid)
一种让神经活动安定的抑制性神经递质。在儿童早期发育中会暂时具有兴奋作用,随着成长转变为抑制功能。
抑制性神经递质(Inhibitory Neurotransmitter)
抑制神经活动的化学物质,GABA是典型代表,可防止过度兴奋,维持大脑平衡。
兴奋—抑制平衡(Excitation/Inhibition Balance, E/I平衡)
指神经活动兴奋与抑制的动态平衡。失衡会导致感官过敏、睡眠紊乱或易发生癫痫。
GABA极性转换(GABA Polarity Shift)
GABA作用随发育从兴奋性转为抑制性的过程。若时机延迟或转换异常,会影响神经回路的形成与发育表现。
氯离子转运体(Chloride Transporter)
调控神经细胞内外Cl⁻浓度的蛋白。KCC2负责Cl⁻外排,NKCC1负责Cl⁻输入,直接参与GABA极性转换。
KCC2(SLC12A5)
将Cl⁻排出神经细胞的转运体,随发育增加,是GABA转向抑制功能所必需的。